Fenylopiracetam i analogi piracetamu – nowe generacje leków prokognitywnych

Streszczenie
Piracetam (2-okso-1-pirolidynoacetamid) zapoczątkował rodzinę tzw. racetamów – związków o wspólnym rdzeniu 2-pirolidonu, dla których przez dekady postulowano działanie prokognitywne, neuroprotekcyjne i modulujące plastyczność synaptyczną. W praktyce klinicznej dowody skuteczności piracetamu w otępieniach i „nieswoistych” zaburzeniach poznawczych okazały się niespójne, co dobrze ilustrują przeglądy Cochrane oraz metaanalizy oparte na wskaźnikach globalnej poprawy. cochranelibrary.com+1 Równolegle rozwijano analogi strukturalne o bardziej specyficznych celach molekularnych (np. lewetyracetam i briwyracetam – ligandy SV2A), a także pochodne o wyraźniejszym komponencie katecholaminergicznym (fenylopiracetam/fonturacetam; enancjomery o profilu inhibitora DAT). PubMed+2SAGE Journals+2 Celem artykułu jest syntetyczne przedstawienie: (1) chemii i zależności struktura-aktywność w obrębie racetamów, (2) współczesnych hipotez mechanistycznych, (3) jakości dowodów klinicznych dla piracetamu i wybranych analogów, (4) bezpieczeństwa, ryzyk oraz kontekstu regulacyjnego (w tym antydopingowego dla fenylopiracetamu). World Anti Doping Agency+1
Uwaga: poniższy tekst ma charakter naukowo-przeglądowy i nie jest poradą medyczną ani rekomendacją stosowania jakichkolwiek substancji.
1. Tło historyczne i definicje: „nootrop” vs „lek prokognitywny”
Termin „nootrop” bywa używany szeroko (obejmując zarówno leki, jak i suplementy), natomiast w ujęciu farmakologicznym sensowniej mówić o lekach prokognitywnych: związkach, które w badaniach kontrolowanych poprawiają wybrane domeny poznawcze lub funkcjonowanie w określonych jednostkach chorobowych, z akceptowalnym profilem bezpieczeństwa. Duża część piśmiennictwa wskazuje, że efekty „prokognitywne” racetamów są bardziej prawdopodobne w stanach upośledzenia (np. po udarze, w otępieniach, w wybranych encefalopatiach) niż u osób zdrowych, a jednocześnie wyniki są heterogeniczne między badaniami. cochranelibrary.com+2SpringerLink+2
2. Chemia rdzenia racetamowego i kierunki modyfikacji
2.1. Rdzeń 2-pirolidonu jako platforma
Piracetam jest prostą pochodną 2-pirolidonu, a wiele „klasycznych racetamów” utrzymuje ten rdzeń, modyfikując:
- podstawnik przy pierścieniu (zwiększenie lipofilowości, przenikania BBB),
- długość/charakter łańcucha amidowego,
- stereochemię (enancjomery o odmiennym powinowactwie do celów białkowych).
Klasyczny przegląd farmakologii racetamów podkreślał, że w modelach zwierzęcych piracetamopodobne związki mogą odwracać amnezję wywołaną m.in. skopolaminą czy niedotlenieniem, lecz translacja do kliniki była zmienna. PubMed
2.2. Zwiększanie lipofilowości i „mocniejszy fenotyp” działania: fenylopiracetam
Fenylopiracetam (fonturacetam; 4-phenylpiracetam) zawiera podstawnik fenylowy zwiększający lipofilowość, co wiązano z silniejszym wpływem na czuwanie/napęd i – w części badań – na parametry poznawcze. Co kluczowe, nowsze prace sugerują, że enancjomery fenylopiracetamu wykazują aktywność w układzie dopaminergicznym poprzez hamowanie transportera dopaminy (DAT), co odróżnia go mechanistycznie od piracetamu. ScienceDirect+1
2.3. Analog piracetamu jako lek o innym przeznaczeniu klinicznym: lewetyracetam i generacje SV2A
Linią rozwojową o największym znaczeniu regulacyjnym jest przejście od „nootropu” do leków przeciwpadaczkowych będących analogami piracetamu:
- Lewetyracetam – analog strukturalny piracetamu; odkrycie i rozwój powiązano z identyfikacją specyficznego miejsca wiązania w mózgu, a następnie celu SV2A (synaptic vesicle protein 2A). PubMed+1
- Briwyracetam – „kolejna generacja” o wyższym powinowactwie do SV2A; szeroko omawiany w przeglądach klinicznych i mechanistycznych jako presynaptyczny modulator uwalniania neurotransmiterów. SAGE Journals+1
To ważny przykład, że „analogi piracetamu” nie muszą być stricte „prokognitywne” w sensie wskazań – mogą reprezentować optymalizację farmakoforu do zupełnie innego celu terapeutycznego.
2.4. Peptydowe i „nietypowe” analogi: GVS-111 oraz unifiram/sunifiram
W literaturze pojawiają się próby odejścia od klasycznego rdzenia w kierunku:
- peptydowych analogów (np. GVS-111) badanych m.in. pod kątem wpływu na prądy kanałów jonowych (Ca²⁺ i K⁺) w neuronach, co miało stanowić potencjalny element mechanizmu prokognitywnego/neuroprotekcyjnego. PubMed+1
- związków opisywanych jako „silniejsze od piracetamu” (np. unifiram DM232 i sunifiram DM235), dla których publikowano dane przedkliniczne i farmakologiczne (odwracanie amnezji w modelach zwierzęcych), jednak bez równoważnego ciężaru dowodów klinicznych i regulacyjnych jak dla leków zatwierdzonych. PMC+1
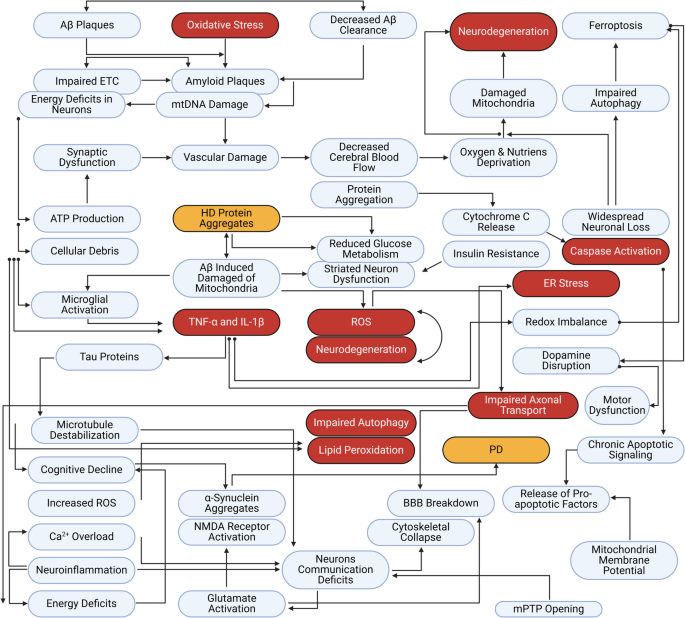
3. Mechanizmy działania: od hipotez „membranowych” do celów molekularnych
3.1. Piracetam – mechanizm wieloczynnikowy i trudny do uchwycenia
Dla piracetamu proponowano m.in.:
- modulację płynności błon, wpływ na funkcje receptorów i transporterów,
- wpływ na metabolizm energetyczny i mikrokrążenie mózgowe,
- modulację neuroprzekaźnictwa cholinergicznego i glutaminergicznego (często pośrednio),
- oddziaływania na kanały jonowe w wysokich stężeniach (w badaniach elektrofizjologicznych).
Część tych wątków wspierały eksperymenty porównujące piracetam i analogi (w tym lewetyracetam) oraz prace dotyczące kanałów jonowych i pochodnych peptydowych. PubMed+1
3.2. Fenylopiracetam – komponent katecholaminergiczny (DAT)
W odróżnieniu od „klasycznego” obrazu piracetamu, fenylopiracetam (szczególnie w ujęciu enancjoselektywnym) został opisany jako inhibitor DAT:
- prace elektrofizjologiczne i amperometryczne wskazywały na właściwości zgodne z hamowaniem transportera dopaminy dla S-fenylopiracetamu oraz różnice między izomerami, ScienceDirect
- badania przedkliniczne opisywały też działania neuroprotekcyjne i przeciwzapalne dla R-fenylopiracetamu, interpretowane w kontekście farmakologii inhibitorów DAT. SpringerLink
- nowsze przeglądy mechanizmów „kognitywnych modulatorów monoamin” włączają fenylopiracetam do grupy związków, których potencjał prokognitywny ma wynikać m.in. z modulacji dopaminergicznej w obwodach czołowo-prążkowiowych. PMC
Implikacja: jeśli DAT jest realnym, istotnym celem fenylopiracetamu, to efekt „prokognitywny” może być w praktyce sprzężony z efektem psychostymulującym (czuwanie, motywacja, napęd), co jednocześnie zmienia profil ryzyk (bezsenność, pobudzenie, wzrost ciśnienia, potencjał nadużywania w wybranych populacjach).
3.3. „Analogi piracetamu” z twardym celem białkowym: SV2A
Najbardziej jednoznaczny mechanistycznie nurt w tej rodzinie to SV2A:
- lewetyracetam – szeroko omawiany jako ligand SV2A z dodatkowymi efektami na homeostazę Ca²⁺ i układy receptorowe, ale „kręgosłupem” pozostaje presynaptyczne oddziaływanie przez SV2A, MDPI
- brivaracetam – lek o tym samym celu, opisywany jako bardziej selektywny/„mocniejszy” w zakresie SV2A w porównaniu do lewetyracetamu w ujęciu farmakologicznym i klinicznym. SAGE Journals+1
To pokazuje, że z chemicznie podobnej platformy można uzyskać substancje o bardzo różnych „fenotypach” klinicznych – od niejednoznacznie prokognitywnych po wysoce skuteczne przeciwpadaczkowe.
4. Dowody kliniczne: piracetam, fenylopiracetam i wybrane racetamy
4.1. Piracetam w otępieniach i zaburzeniach poznawczych wieku podeszłego
Cochrane (przeglądy dotyczące otępienia lub zaburzeń poznawczych) wskazywały, że opublikowane dowody nie wspierają rutynowego stosowania piracetamu w leczeniu otępienia, mimo że w części badań widziano sygnał w miarach globalnej poprawy; brakowało natomiast spójnych korzyści w bardziej specyficznych testach poznawczych. cochranelibrary.com+1
Jednocześnie metaanaliza obejmująca wiele badań podwójnie ślepych z placebo opisywała różnicę na korzyść piracetamu w globalnym wrażeniu klinicznym poprawy, co ilustruje napięcie między „miękkimi” miarami klinicznymi a twardszymi domenami neuropsychologicznymi. PubMed+1
W klasycznych badaniach długoterminowych w chorobie Alzheimera raportowano hipotezę możliwego spowolnienia pogorszenia w wybranych miarach pamięci przy wysokich dawkach i długim podawaniu, jednak nie był to przełom prowadzący do szerokich rekomendacji. PubMed
Wniosek praktyczny z literatury: piracetam może dawać niejednorodny sygnał kliniczny w heterogenicznych populacjach „zaburzeń poznawczych”, ale jakość i spójność efektów w twardych punktach końcowych nie uzasadnia traktowania go jako leku o ugruntowanej skuteczności w otępieniach.
4.2. Piracetam po udarze: afazja
W obszarze rehabilitacji po udarze piracetam badano m.in. w afazji:
- RCT i badania wieloośrodkowe sugerowały możliwy efekt wspomagający rehabilitację językową w części populacji, ScienceDirect+1
- jednak nowsza metaanaliza RCT wskazywała na ograniczoną rolę: potencjalnie korzyść bardziej w domenie pisania niż w ogólnej ciężkości afazji, a efekt może słabnąć w czasie. PubMed+1
Interpretacja: jeśli efekt istnieje, może być specyficzny, zależny od intensywnej terapii językowej i rodzaju mierzonej funkcji.
4.3. Aniracetam i oxiracetam – dane kliniczne mieszane
Dla aniracetamu publikowano badania randomizowane u pacjentów z otępieniem typu alzheimerowskiego lub pogorszeniem funkcji poznawczych, z pewnymi sygnałami poprawy w skalach klinicznych/behawioralnych w części prac, ale również z doniesieniami o działaniach niepożądanych (np. epizody splątania u części chorych). PubMed+2SpringerLink+2
Dla oxiracetamu istnieją współczesne próby kliniczne (np. w zaburzeniach poznawczych po udarze) projektowane jako badania randomizowane; dostępne streszczenia i protokoły wskazują, że to obszar nadal „w toku”, bez jednoznacznego standardu leczenia opartego o racetamy. PubMed+1
4.4. Fenylopiracetam: luka między farmakologią a kliniką w literaturze międzynarodowej
W porównaniu do piracetamu, fenylopiracetam ma relatywnie mocniejszą, nowocześniej opisaną farmakologię (DAT; różnice enancjomerów), ale mniej powszechnie dostępnych w zachodnich bazach danych dużych, wysokiej jakości RCT oceniających „czyste” punkty poznawcze w precyzyjnych wskazaniach. Najczęściej cytowane są:
- badania przedkliniczne dokumentujące profil inhibitora DAT i efekty neurobehawioralne, ScienceDirect+1
- prace opisujące potencjał neuroprotekcyjny/przeciwzapalny (modele zwierzęce), SpringerLink
- przeglądy łączące fenylopiracetam z grupą „modulatorów monoamin” w kontekście uczenia i funkcji wykonawczych. PMC
Konkluzja oparta o stan dowodów: fenylopiracetam jest interesujący jako „racetam o jawnej osi dopaminergicznej”, ale klinicznie – w rygorze EBM – pozostaje trudniejszy do jednoznacznej oceny jako lek prokognitywny, zwłaszcza poza krajami, gdzie był szerzej stosowany.
5. Bezpieczeństwo, ryzyka i kontekst regulacyjny
5.1. Bezpieczeństwo kliniczne piracetamu
Piracetam jest generalnie opisywany jako dobrze tolerowany w wielu badaniach, ale profil działań niepożądanych zależy od populacji, dawki i chorób współistniejących. Wskazania i status rejestracyjny różnią się między krajami, a część zastosowań ma charakter historyczny/off-label.
5.2. Fenylopiracetam jako substancja o statusie stymulantu w sporcie
Fenylopiracetam/fonturacetam jest istotny z perspektywy sportu i regulacji:
- WADA publikuje coroczną Listę Substancji i Metod Zabronionych; stymulanty (kategoria S6) obejmują m.in. fonturacetam (4-phenylpiracetam/carphedon) w wielu wersjach list w ostatnich latach. World Anti Doping Agency+1
- przeglądy dotyczące „nieautoryzowanych składników” w suplementach nootropowych oraz ryzyk dopingowych omawiają fenylopiracetam jako przykład związku obecnego w obrocie konsumenckim i problematycznego regulacyjnie. PubMed+1
- w 2025 r. opublikowano też analizę pojęcia „brain doping” i trudności interpretacyjnych wynikających z otwartego charakteru listy i zmienności rynku suplementów. PMC+1
Wniosek: w sporcie wyczynowym fenylopiracetam ma realne konsekwencje antydopingowe, a ponadto jego mechanizm (DAT) jest spójny z fenotypem stymulantu.
6. „Nowe generacje” – co faktycznie znaczy postęp w tej klasie?
W literaturze można wyróżnić trzy sensowne osie „nowej generacji”:
- Urealnienie celu molekularnego
Największy postęp nastąpił tam, gdzie analogi piracetamu przestały być „nieswoistymi nootropami”, a stały się lekami o twardym celu (SV2A) i twardych punktach końcowych (kontrola napadów): lewetyracetam/brivaracetam. MDPI+1 - Enancjoselektywność i „farmakologia dopaminowa”
Fenylopiracetam pokazuje, że stereochemia może nie tylko „podkręcać moc”, ale zmieniać całą klasę mechanizmu (w stronę inhibitorów DAT) – co ma konsekwencje poznawcze, behawioralne i bezpieczeństwa. ScienceDirect+1 - Racjonalne poszukiwanie markerów odpowiedzi i populacji docelowych
Dla piracetamu i części racetamów problemem nie musi być „brak działania”, ale brak precyzyjnej stratyfikacji: różne fenotypy pacjentów, różne domeny poznawcze, różne interwencje towarzyszące (np. intensywność terapii w afazji) i różne miary efektu (globalne wrażenie vs testy domenowe). Metaanalizy w afazji i otępieniach pokazują, że wybór punktów końcowych potrafi zmienić wniosek kliniczny. SpringerLink+1
7. Kierunki badań (wnioski i hipotezy)
Na podstawie dostępnych prac naukowych najbardziej obiecujące (metodologicznie) kierunki to:
- Projektowanie analogów z jednoznacznym targetem (jak SV2A) zamiast „wieloczynnikowych” nootropów bez biomarkerów odpowiedzi. MDPI+1
- Badania enancjomerów fenylopiracetamu osobno (R vs S), z jasnym rozdzieleniem efektów czuwania/napędu od stricte poznawczych. ScienceDirect+1
- Lepsze, domenowe punkty końcowe (np. funkcje wykonawcze, pamięć robocza, specyficzne komponenty językowe w afazji) i protokoły łączące farmakoterapię z rehabilitacją, tam gdzie to ma sens kliniczny. ScienceDirect+1
- Kontrola jakości rynku „nootropików”: prace z neurologii i toksykologii pokazują, że w produktach „cognitive enhancement” mogą występować niezadeklarowane, niezatwierdzone substancje (w tym racetamy), co komplikuje zarówno bezpieczeństwo pacjenta, jak i interpretację doniesień „z życia”. Neurology+2PubMed+2
Bibliografia
- Gouliaev AH, Senning A. Piracetam and other structurally related nootropics. Brain Res Brain Res Rev. 1994. PubMed
- Flicker L, Grimley Evans G. Piracetam for dementia or cognitive impairment (Cochrane Review; full text). cochranelibrary.com+1
- Waegemans T, Wilsher CR, Danniau A, Ferris SH, Kurz A, Winblad B. Clinical efficacy of piracetam in cognitive impairment: a meta-analysis. Dement Geriatr Cogn Disord. 2002. Karger Publishers+1
- Croisile B, et al. Long-term and high-dose piracetam treatment… (Alzheimer’s disease). 1993. PubMed
- Zhang J, Wei R, Chen Z, Luo B. Piracetam for Aphasia in Post-stroke Patients: A Systematic Review and Meta-analysis of RCTs. CNS Drugs. 2016. SpringerLink+1
- Huber W, et al. Piracetam as an adjuvant to language therapy for aphasia. 1997. ScienceDirect
- Federici M, et al. Electrophysiological and amperometric evidence… S-phenylpiracetam is a selective DAT inhibitor… Neuropharmacology. 2013. ScienceDirect
- Zvejniece L, et al. S-phenylpiracetam… (badania przedkliniczne; DAT). 2017. ScienceDirect
- (R)-PhP – Neuroprotective and anti-inflammatory activity… 2020. SpringerLink
- Boyle N, et al. Monoaminergic Modulation of Learning and Cognitive… 2024 (przegląd, w tym fenylopiracetam/DAT). PMC
- Kenda BM, et al. Discovery of 4-substituted pyrrolidone butanamides… (lewetyracetam jako analog piracetamu). J Med Chem. 2004. PubMed+1
- Contreras-García IJ, et al. Levetiracetam Mechanisms of Action: From Molecules to Systems. Pharmaceutics. 2022. MDPI
- Steinhoff BJ. Levetiracetam and brivaracetam: a review of evidence… 2019. SAGE Journals
- Solntseva EI, et al. The effects of piracetam and its novel peptide analogue GVS-111 on neuronal voltage-gated calcium and potassium channels. Gen Pharmacol. 1997. PubMed+1
- Romanelli MN, et al. Pharmacological Characterization of DM232 (Unifiram) and DM235 (Sunifiram)… 2006. PMC+1
- Cohen PA, et al. Five Unapproved Drugs Found in Cognitive Enhancement Supplements. Neurology: Clinical Practice. 2021. Neurology
- Jędrejko K, et al. Unauthorized ingredients in “nootropic” dietary supplements… 2023. PubMed
- World Anti-Doping Agency (WADA). 2025 Prohibited List (PDF). World Anti Doping Agency+1
- Vanhee C, et al. The Occurrence of Illicit Smart Drugs… market surveillance study by medicines control laboratories. J Xenobiotics. 2025. MDPI
- Pokrywka A, et al. “Brain doping” substances: prohibited or not in sports? Biol Sport. 2025. PMC+1
Opracowanie: Rafał Klasiński – Fundacja Independent Institute of Chemical Processes