Wprowadzenie
Leki mające działać w ośrodkowym układzie nerwowym (OUN) muszą pokonać wyjątkowo restrykcyjną barierę krew–mózg (BBB, ang. blood–brain barrier). BBB stanowi półprzepuszczalną granicę między krążeniem ogólnym a tkanką nerwową, która chroni mózg przed toksynami i patogenami. Niestety ta sama bariera silnie utrudnia dostarczanie farmaceutyków do mózgu – szacuje się, że ponad 98% małocząsteczkowych leków oraz praktycznie wszystkie leki wielkocząsteczkowe nie mogą swobodnie przeniknąć do OUN. Skutkiem tego rozwój farmakoterapii chorób mózgu napotyka ogromne trudności – około 95% kandydatów na leki neurologiczne odpada już na etapie badań przedklinicznych z powodu niewystarczającej przepuszczalności przez BBB. W niniejszym artykule omówiono budowę i funkcje bariery krew–mózg, wyzwania związane z przenikaniem leków przez BBB oraz najnowsze strategie projektowania związków i systemów dostarczających leki do mózgu. Szczególny nacisk położono na mechanizmy umożliwiające pokonanie BBB, w tym modyfikacje chemiczne leków, wykorzystanie nośników nanotechnologicznych, technologię nanoprzeciwciał oraz układy transportujące. Przedstawiono także przykłady konkretnych leków stosowanych w terapii chorób neurodegeneracyjnych (Alzheimera, Parkinsona, SLA) wraz z mechanizmami ich przenikania przez BBB, a także przegląd aktualnych patentów i badań nad nowymi metodami dostarczania leków do mózgu.
Budowa i funkcja bariery krew–mózg (BBB)
BBB jest wyspecjalizowaną, dynamiczną barierą fizjologiczną oddzielającą krew od płynu zewnątrzkomórkowego mózgu. Tworzy ją neurokompleks naczyniowy (ang. neurovascular unit, NVU), na który składają się komórki śródbłonka naczyń włosowatych mózgu, otaczające je pericyty, błona podstawna naczyń oraz tzw. stopki okołonaczyniowe astrocytów. Komórki śródbłonka mózgowego pełnią kluczową rolę – ściśle do siebie przylegają za pomocą połączeń zamykających (ścisłych) utworzonych przez białka takie jak klaudyny, okludyny i JAM, co uniemożliwia parakomórkowy przeciek substancji między komórkami. W przeciwieństwie do śródbłonka obwodowego, komórki te nie mają fenestracji (okienek), a ich błony dzielą się na odrębne domeny luminalną i abluminalną dzięki obecności zarówno połączeń ścisłych, jak i przylegających. Śródbłonek ten charakteryzuje się również wysoką aktywnością metaboliczną – zawiera liczne mitochondria zapewniające energię do transportu aktywnego.
Otaczające śródbłonek pericyty wnikają w błonę podstawną i poprzez sygnały (np. TGF-β, VEGF) regulują przepuszczalność i integrację połączeń ścisłych. Astrocyty ze swoimi wypustkami okalają ponad 90% obwodu naczyń włosowatych mózgu. Wydzielają czynniki wzrostowe (np. BDNF) wspierające dojrzewanie śródbłonka i utrzymanie bariery, a także reagują na potrzeby metaboliczne neuronów, pośrednio wpływając na transport substancji przez BBB. Całość uzupełnia błona podstawna z kolagenem i lamininą, zapewniając strukturalne wsparcie naczyń oraz platformę sygnałową dla interakcji między śródbłonkiem a pericytami.
Fizjologiczną funkcją BBB jest ochrona i homeostaza – zapobieganie przedostawaniu się szkodliwych czynników z krwi do mózgu przy jednoczesnym zapewnieniu dostępu dla niezbędnych składników odżywczych. Liczne transportery błonowe obecne na komórkach śródbłonka odpowiadają za selektywny transport potrzebnych substancji (np. transportery glukozy GLUT1, aminokwasów LAT1, transportery jonowe). Z kolei aktywne pompy efluksowe (głównie z rodziny białek ABC, jak P-gp – glikoproteina P/ABCB1, BCRP – breast cancer resistance protein, i białka MRP) chronią mózg przed xenobiotykami, usuwając z komórek śródbłonka wiele związków zanim przenikną do tkanki nerwowej. Te mechanizmy sprawiają, że zdrowa BBB jest wysoce selektywna – preferencyjnie przepuszcza małe cząsteczki niepolarne i substancje niezbędne, odfiltrowując większość pozostałych. Przykładowo, do mózgu na drodze dyfuzji biernej przenikają tylko związki lipofilowe o masie <~400–500 Da i odpowiednio małej polarności (np. logP > 2, ≤5–6 wiązań wodorowych). Większe lub bardziej polarne molekuły wymagają specjalnych mechanizmów transportu bądź pozostają zatrzymane.
BBB pełni też rolę bariery metabolicznej – komórki śródbłonka posiadają enzymy (np. monoaminooksydazy, peptydazy) zdolne rozkładać niektóre cząsteczki zanim przedostaną się dalej. W ten sposób bariera krew–mózg dba o stałość składu płynu mózgowego, chroniąc neurony przed wahaniami stężeń hormonów, toksyn czy neuroprzekaźników krążących we krwi.
W warunkach patologicznych integralność BBB może ulec zaburzeniu. W udarach, stwardnieniu rozsianym, urazach mózgu czy zaawansowanych chorobach neurodegeneracyjnych obserwuje się rozszczelnienie bariery krew–mózg, skutkujące obrzękiem, napływem komórek zapalnych i dysregulacją homeostazy jonowej. Przykładowo u pacjentów z chorobą Alzheimera i Parkinsona stwierdzano zmiany w ekspresji białek połączeń ścisłych i zwiększoną reaktywność zapalną śródbłonka, co może pogłębiać uszkodzenia neuronów. Paradoksalnie jednak nawet częściowa degradacja BBB w tych schorzeniach nie rozwiązuje problemu dostarczania leków – bariera pozostaje wystarczająco selektywna, by wciąż stanowić przeszkodę dla terapii, a jednocześnie jej uszkodzenie może mieć negatywne skutki dla funkcjonowania mózgu.
Wyzwania związane z przenikaniem leków przez BBB
Efektywne dostarczenie leku do mózgu stanowi jedno z największych wyzwań we współczesnym projektowaniu farmaceutyków. Ścisła struktura BBB i jej system transportowy sprawiają, że ogromna większość cząsteczek farmakologicznie czynnych nie osiąga terapeutycznych stężeń w OUN. Tradycyjne małe cząsteczki lecznicze muszą spełnić rygorystyczne kryteria fizykochemiczne, aby biernie dyfundować przez barierę – m.in. niewielki rozmiar (<500 Da) i odpowiednią lipofilowość. Nawet spełnienie tych warunków nie gwarantuje sukcesu, ponieważ aktywne mechanizmy odpływu mogą usuwać lek z powrotem do krwi. Glikoproteina P (P-gp) oraz inne pompy efluksowe w komórkach śródbłonka rozpoznają wiele strukturalnie różnych cząsteczek (np. leki przeciwnowotworowe, antybiotyki, leki psychotropowe) i aktywnie je eksportują, ograniczając ich wewnątrzmózgowe stężenie. Na przykład crizotinib – inhibitor kinazy ALK stosowany w onkologii – wykazuje znikome stężenie w mózgu pomimo odpowiedniej lipofilowości, właśnie z powodu działania P-gp. Z kolei donepezil – klasyczny inhibitor acetylocholinoesterazy w chorobie Alzheimera – choć dość swobodnie przenika do OUN dzięki niewielkim rozmiarom i lipofilowości, jest częściowo usuwany przez P-gp, co ogranicza jego akumulację w mózgu. Badania na myszach z nokautem genu Mdr1a (kodującego P-gp) wykazały blisko 2,4-krotnie wyższe stężenie donepezilu w mózgu niż u zwierząt z prawidłową ekspresją P-gp, dowodząc roli tego transportera w farmakokinetyce leku. Podobnie riluzol – lek spowalniający przebieg SLA – jest substratem zarówno P-gp, jak i BCRP; hamowanie tych pomp lub ich genetyczny brak zwiększa przenikanie riluzolu do mózgu 1,4–2,1 raza. W modelach zwierzęcych SLA stwierdzono wręcz nadekspresję P-gp w naczyniach mózgowych, co może przyczyniać się do słabszej skuteczności leków.
Zwiększenie lipofilowości leku bywa intuicyjnym podejściem do poprawy przepuszczalności przez BBB. Rzeczywiście, modyfikacje strukturalne zwiększające rozpuszczalność w tłuszczach mogą nasilać dyfuzję przez barierę – np. dodanie grupy fluoroetylowej do crizotinibu znacząco polepszyło jego przenikanie do mózgu. Jednak strategia ta ma ograniczenia: nadmierna lipofilowość może skutkować utratą selektywności i aktywności biologicznej leku oraz zwiększoną kumulacją w tkankach obwodowych, co potęguje działania niepożądane. Ponadto skrajnie hydrofobowe cząsteczki często silnie wiążą się z białkami krwi i magazynują w tkance tłuszczowej, zmniejszając ilość docierającą do mózgu.
Kolejnym wyzwaniem jest wielkość cząsteczki. Nowoczesne terapie, takie jak przeciwciała monoklonalne, fragmenty antygenowe, peptydy czy oligonukleotydy, cechują się masą od kilku do kilkudziesięciu kDa, co praktycznie uniemożliwia przeniknięcie przez nienaruszoną BBB na drodze dyfuzji. Standardowe przeciwciało IgG (~150 kDa) przenika do mózgu w ułamku procenta podanej dawki – dla uzyskania efektu terapeutycznego konieczne jest więc podawanie bardzo wysokich dawek systemowych, co zwiększa koszty i ryzyko działań niepożądanych.
Heterogenność i dynamiczność BBB stanowi kolejną komplikację. Bariera krew–mózg nie jest jednakowa we wszystkich obszarach mózgu i może zmieniać się pod wpływem czynników takich jak stan zapalny, stres oksydacyjny czy starzenie. Ponadto niektóre regiony (np. narząd podsklepieniowy, obszar postrema) są fizjologicznie pozbawione ścisłej bariery, co jednak wykorzystuje organizm raczej do celów czuciowych (monitorowania składu krwi) niż jako drogi dostarczania leków. Z punktu widzenia terapii, dynamiczne zmiany w ekspresji transporterów czy przepuszczalności BBB (np. w przebiegu neurozapalenia) mogą wpływać na zmienną skuteczność leków w czasie choroby.
Wobec powyższych przeszkód, skuteczne leczenie chorób OUN wymaga przemyślanego projektowania leków i systemów dostarczania, które zdołają ominąć lub przechytrzyć barierę krew–mózg. W następnej sekcji przedstawiono strategie, jakie opracowano w celu zwiększenia transportu farmaceutyków do mózgu, z wykorzystaniem wiedzy o mechanizmach przenikania przez BBB.
Strategie projektowania leków penetrujących BBB
Pomimo nieprzepuszczalności BBB dla większości związków, istnieją fizjologiczne szlaki transportowe, które można wykorzystać do dostarczania leków do mózgu. Nowoczesne podejścia projektowania leków często naśladują naturalne mechanizmy przenikania przez barierę lub czasowo ją modyfikują. Poniżej omówiono najważniejsze strategie, w tym modyfikacje chemiczne cząsteczek, systemy nośnikowe (nanonośniki), technologie nanoprzeciwciał (single-domain) oraz wykorzystanie transporterów i receptorów BBB, jak również metody alternatywne (np. dostarczanie donosowe, fizyczne otwieranie bariery).
Modyfikacje chemiczne leku: Klasycznym podejściem jest ulepszanie właściwości cząsteczki tak, by łatwiej przeniknęła ona przez BBB. Obejmuje to zwiększanie lipofilowości (przez dodanie grup hydrofobowych), zmniejszanie rozmiaru cząsteczki, redukcję liczby polarnych ugrupowań (np. grup –OH, –NH) czy maskowanie ładunku. Tworzenie proleków aktywowanych dopiero w mózgu to częsta praktyka – hydrofilowa grupa polarna leku jest czasowo zestryfikowana lub związana z innym fragmentem, co ułatwia przekroczenie bariery, a dopiero w OUN następuje odtworzenie aktywnej postaci. Przykładem może być diacetylowa pochodna morfiny – heroina – która znacznie szybciej przenika do mózgu niż wolna morfina, po czym ulega enzymatycznej deacetylacji do aktywnego metabolitu. Innym podejściem jest maskowanie ładunku elektrycznego – np. dodanie hydrofobowej grupy osłaniającej jonizowalną funkcję amonową czy karboksylową leku, by zmniejszyć jego polarność. Należy jednak pamiętać, że modyfikacje takie nie mogą istotnie upośledzać wiązania leku z celem molekularnym. Ponadto, jak wspomniano, nadmierne uhydrofobienie cząsteczki może prowadzić do niespecyficznej dystrybucji i toksyczności obwodowej. Dlatego projektowanie proleków zakłada zwykle odwracalne modyfikacje – np. dodanie fragmentu fosforanowego poprawiającego rozpuszczalność, który po przejściu BBB jest odcinany przez fosfatazy (strategie stosowane m.in. dla nukleozydowych leków przeciwwirusowych i chemioterapeutyków).
Wykorzystanie transporterów (transportery ułatwione): Komórki śródbłonka BBB posiadają liczne białka przenośnikowe dla ważnych substancji odżywczych – ten fakt można wykorzystać, projektując leki „podszywające się” pod naturalne substraty tych transporterów. Przykładem jest L-DOPA (lewodopa), prekursor dopaminy stosowany w chorobie Parkinsona. Lewodopa strukturalnie przypomina duży obojętny aminokwas i jest transportowana przez system LAT1 (L-type amino acid transporter) obecny na BBB. Dzięki temu może skutecznie dotrzeć do mózgu, gdzie ulega dekarboksylacji do dopaminy – co więcej, podawanie jej z inhibitorem dekarboksylazy (karbidopą) zapobiega przedwczesnej konwersji na obwodzie, zwiększając ilość dostępnego substratu dla transportera LAT1. Innym przykładem jest wykorzystanie transporterów glukozy (GLUT1) – do cząsteczki leku można dołączyć resztę cukrową lub utworzyć koniugat z glukozą, by ułatwić absorpcję przez śródbłonek (tę strategię badano np. dla analogów leków przeciwwirusowych oraz peptydów). Podobnie, witamina B6 i kwas foliowy mają swoje transportery – powstały koniugaty folianowe leków przeciwnowotworowych skierowanych do mózgu. Ważne jest precyzyjne dopasowanie – modyfikacja leku nie może uniemożliwić rozpoznania przez transporter ani spowodować jego uwięźnięcia w komórce śródbłonka.
Transcytoza receptorowa (układ „trojańskiego konia”): Mózg potrzebuje nie tylko drobnych cząstek, ale i większych, jak transferyna, insulina, leptyna czy IgG matczyne – i posiada dla nich receptory na powierzchni śródbłonka. Mechanizm receptor-mediate transcytosis (RMT) można wykorzystać konstruując leki lub nośniki wyposażone w ligandy wiążące te receptory. Klasycznym celem jest receptor transferynowy (TfR) – liczne badania wykazały, że dołączenie do leku nanocząstki lub przeciwciała ligandu TfR (np. samej transferyny, przeciwciała anty-TfR lub fragmentu wiążącego receptor) pozwala na „przemycenie” leku przez komórkę śródbłonka na drodze endocytozy i egzocytozy po stronie mózgowej. Podobnie wykorzystywano receptor insulinowy czy LRP1 (low-density lipoprotein receptor-related protein 1, który transportuje m.in. apolipoproteiny i Angiopep-2). Przykładem zastosowania jest koniugat paclitakselu z peptydem Angiopep-2 (ang. ANG1005) opracowany w celu leczenia przerzutów nowotworowych do mózgu – Angiopep-2 wiąże LRP1, co stymuluje przeniesienie cząsteczki przez BBB. Strategię RMT wykorzystano także w nowatorskich terapiach przeciw chorobie Alzheimera: stworzono bispecyficzne przeciwciała mające dwie różne domeny – jedna rozpoznaje docelowy antygen (np. β-amyloid), a druga wiąże się z receptorem na BBB (np. TfR). Taki „antyciałowy konik trojański” jest transportowany przez barierę i dostarcza lek (przeciwciało) do mózgu. Firma Roche opracowała platformę Brain Shuttle, gdzie przeciwciało anty-Aβ zostało zmodyfikowane fragmentem wiążącym TfR, co znacząco zwiększyło ilość leku w mózgu w porównaniu do tradycyjnego przeciwciała. W 2022 r. ogłoszono także przyznanie patentu na platformę szwedzkiej firmy BioArctic, umożliwiającą transport biotherapeutyków (np. przeciwciał) przez BBB – technologia ta ma poprawić skuteczność i ograniczyć działania niepożądane leczenia chorób neurodegeneracyjnych.
Nanoprzeciwciała (single-domain antibodies): Szczególnym przypadkiem podejścia opartego o przeciwciała są tzw. nanoprzeciwciała, czyli jednodomenowe fragmenty przeciwciał (typowo pochodzące z układu odpornościowego wielbłądowatych). Mają one masę ok. 15 kDa (czyli ~1/10 pełnego IgG) i rozmiar nanometryczny, co może sprzyjać dyfuzji przez BBB oraz lepszej penetracji tkanki mózgowej. Nanoprzeciwciała cechują się wysokim powinowactwem i niską immunogennością, a ponadto łatwo je modyfikować genetycznie. Same z siebie wciąż przenikają przez barierę w ograniczonym stopniu (15 kDa to wciąż ponad granicę swobodnej dyfuzji, a dodatkowo większość nanociał jest dość hydrofilowa), jednak dzięki niewielkim rozmiarom można sprytnie je dostarczać różnymi metodami: jako komponent wirusowych wektorów genowych, w formie fuzji z peptydami kierującymi do receptorów BBB, czy w koniugatach z nanonośnikami. Przykładowo, opisano dwuwalentne nanoprzeciwciało anty-NMDA podane obwodowo u myszy – w badaniu wykazano, że była w stanie przeniknąć do mózgu i poprawić funkcje poznawcze w modelu choroby neurodegeneracyjnej. Zaletą nanoprzeciwciał jest też krótszy czas krążenia we krwi (brak fragmentu Fc wydłużającego półtrwanie), co zmniejsza ryzyko działań ogólnoustrojowych – to korzystne np. w obrazowaniu PET, gdzie szybko klirens pozwala uzyskać lepszy kontrast mózgowy. Obecnie prowadzi się badania nad nanoprzeciwciałami celującymi w patologie Alzheimera (Aβ, białko tau) i Parkinsona (alfa-synukleina), a także nad połączeniem nanociał z nośnikami – np. sprzężenie nanoprzeciwciała z nanocząstką ferrytową lub radioznacznikiem umożliwia precyzyjne dostarczanie takiego kompleksu i monitorowanie jego penetracji do mózgu.
Nanonośniki i systemy dostarczania: Rewolucja w nanotechnologii dostarczyła całego wachlarza nanonośników, które mogą pełnić rolę „koni trojańskich” dla leków, maskując je przed BBB lub aktywnie ułatwiając transport. Wykorzystuje się zarówno nanomateriały organiczne, jak i nieorganiczne: liposomy, polimerowe nanokapsułki, mikrosfery, hydrożele, dendrymery, nanocząstki metaliczne (np. złota, tlenków żelaza), nanoformulaacje krzemionkowe, węglowe (fulereny, nanorurki), a także struktury pochodzenia biologicznego – egzosomy, wirusy, bakterie. Kluczowym aspektem jest nadanie takim nośnikom zdolności do przekroczenia BBB. Często łączy się kilka strategii: np. PEGylowane liposomy z doczepionym glutationem (wykorzystujące transporter GSH i zmniejszające rozpoznanie przez układ immunologiczny) wykazują podwyższoną penetrację do mózgu. Inne liposomy powlekane polysorbatem 80 wiążą apolipoproteiny z krwi, co sprzyja internalizacji przez receptory LRP na BBB – tak dostarczano do mózgu np. doksorubicynę w modelach glejaka. Nanocząstki polimerowe (PLGA, polikrylonitryl) mogą być funkcjonalizowane ligandami (np. transferryną, peptydem Angiopep-2) lub cząsteczkami adresującymi (np. przeciwciałem anty-TfR), by wykorzystać szlak RMT analogicznie jak opisano wyżej. Nanocząstki magnetyczne umożliwiają z kolei ukierunkowanie leku do określonego obszaru mózgu za pomocą zewnętrznego pola magnetycznego. Egzosomy – biologiczne pęcherzyki wydzielane przez komórki – budzą szczególne zainteresowanie jako nośniki, ponieważ naturalnie uczestniczą w komunikacji międzykomórkowej, w tym potrafią przekraczać bariery fizjologiczne. Patent CN114642736A opisuje wykorzystanie egzosomów neutrofilowych jako nanotransporterów leków do OUN – dzięki właściwościom neutrofili pęcherzyki te przenikają przez BBB i kierują się do ognisk zapalnych w mózgu. W modelach zwierzęcych wykazano, że egzosomalny system dostarczania zwiększa przenikanie leków (np. doksorubicyny, paklitakselu) do tkanki guza glejaka, jednocześnie cechując się dobrą biokompatybilnością. Obecnie trwają prace nad standaryzacją metod izolacji i modyfikacji egzosomów oraz oceną ich bezpieczeństwa.
Transcytoza adsorpcyjna: Innym mechanizmem jest nieswoista transcytoza adsorpcyjna (AMT), w której dodatnio naładowane cząsteczki wiążą się elektrostatycznie do ujemnych składników błony komórek śródbłonka, indukując endocytozę. Tę drogę wykorzystują m.in. polikationowe peptydy przenikające komórki (CPP), takie jak penetratyna czy TAT, a także kationizowana albumina. Konjugacja leku z takim kationowym nośnikiem może zwiększyć jego wychwyt przez śródbłonek i transcytozę do mózgu. Wadą bywa niska selektywność – dodatnio naładowane kompleksy mogą odkładać się nieswoiście także w innych tkankach, a przy większych dawkach uszkadzać komórki. Niemniej, trwają badania nad optymalizacją tego procesu, np. poprzez tworzenie peptydów zwłaszcza aktywowanych w środowisku BBB lub łączenie strategii adsorpcyjnej z receptorową (nadawanie cząsteczce jednocześnie ładunku i powinowactwa do receptorów).
Omijanie lub czasowe otwarcie BBB: Zamiast zmuszać cząsteczki do przekraczania bariery, można dostarczyć lek z pominięciem BBB lub chwilowo ją otworzyć. Jedną z obiecujących dróg jest podawanie donosowe. Wykorzystuje ono bezpośrednie połączenia nerwowe między jamą nosową a OUN – leki aplikowane aerozolem do nosa mogą dyfundować wzdłuż nerwu węchowego i trójdzielnego do opuszki węchowej i pnia mózgu, omijając krążenie systemowe. Ta metoda badana jest m.in. dla insuliny (w celu poprawy funkcji poznawczych w chorobie Alzheimera) oraz dla peptydowych czynników troficznych. Donosowe podanie omija barierę krew–mózg, ale zmaga się z innymi wyzwaniami – ograniczoną objętością dawki, klirensem śluzówkowym i zmiennością osobniczą anatomii nosa. Niemniej, trwają prace nad specjalnymi urządzeniami do aplikacji donosowej oraz formułami (np. żele termożelujące), które przedłużają kontakt leku z nabłonkiem węchowym.
Inną metodą jest czasowe, odwracalne otwarcie BBB za pomocą środków fizycznych lub chemicznych. Klasyczna technika stosowana w onkologii to infuzja hipertonicznego roztworu mannitolu do tętnicy szyjnej – powoduje to osmotyczne obkurczenie komórek śródbłonka i rozluźnienie połączeń ścisłych na kilka godzin, co pozwala wprowadzić leki (np. metotreksat w leczeniu chłoniaków OUN). Bardziej precyzyjną i nieinwazyjną metodą jest skupiona ultrasonografia (FUS) z mikropęcherzykami kontrastu. Ultradźwięki skierowane na wybrany obszar mózgu powodują drgania pęcherzyków w krążeniu, co mechanicznie zwiększa przepuszczalność lokalnych naczyń, umożliwiając przenikanie leków w ciągu kilkudziesięciu minut. Metoda ta była testowana klinicznie m.in. u chorych z chorobą Alzheimera – tymczasowe otwarcie BBB w okolicy kory czołowej pozwoliło na lepszą penetrację podanych dożylnie przeciwciał anty-amyloidowych do tkanki mózgowej, bez poważnych działań niepożądanych. Trwają również badania nad zastosowaniem FUS w SLA (ukierunkowane na korę ruchową lub rdzeń kręgowy). Inne strategie obejmują stosowanie modulatorów chemicznych rozszczelniających barierę (np. bradykininy i analogów jak Cereport/RMP-7, które przejściowo zwiększają przepuszczalność naczyń) czy techniki konwekcyjne (bezpośrednia infuzja leku do miąższu mózgu za pomocą pomp – CED, ang. convection-enhanced delivery). Te ostatnie nie są wprawdzie metodą przekraczania BBB per se, lecz sposobem jej obejścia przez lokalną inwazyjną administrację.
Powyższe strategie często łączone są w hybrydowe systemy dla uzyskania lepszego efektu. Na przykład, podanie nanocząstek złota sprzężonych z peptydem przenikającym (AMT) i ligandem TfR (RMT) może synergicznie zwiększyć transport do mózgu. Nowe koncepcje obejmują także inżynierię komórek zdolnych do migracji przez BBB (np. zmodyfikowane limfocyty T lub makrofagi jako „wehikuły” dostarczające leki w głąb OUN). Trzeba podkreślić, że choć dziesiątki tych metod sprawdziły się w modelach doświadczalnych, stosunkowo niewiele zostało dotąd zatwierdzonych w rutynowej klinice. Niemniej jednak, kilka przykładów leków pokonujących BBB znajduje już zastosowanie terapeutyczne, szczególnie w leczeniu chorób neurodegeneracyjnych.
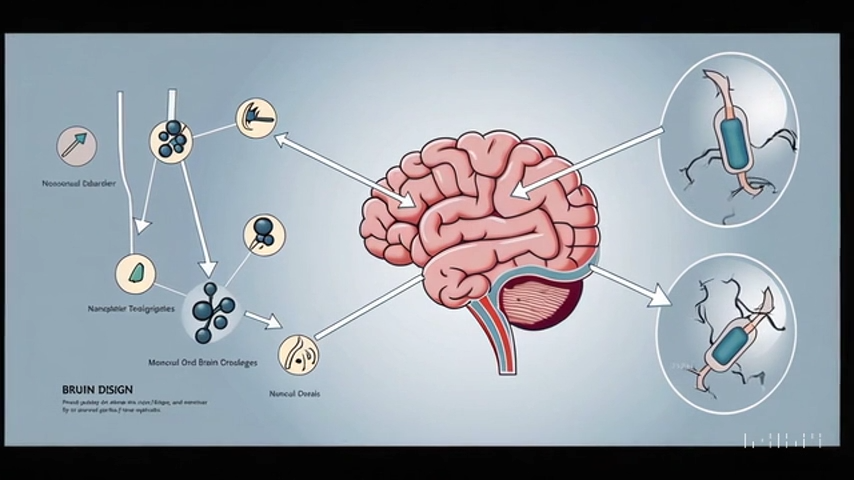
Figura 1: Przykładowe mechanizmy i strategie pokonywania bariery krew–mózg. (a) Schemat mechanizmów transportu przez BBB, w tym dyfuzji biernej lipidowych małych cząsteczek (1), działania pomp efluksowych (2), transcytozy przez wyspecjalizowane transportery (3), transcytozy receptorowej (4), transcytozy komórkowej z udziałem migrujących komórek układu odpornościowego (5), transcytozy adsorpcyjnej dla polikationów (6) oraz ograniczonego transportu parakomórkowego (7) – połączenia ścisłe uniemożliwiają swobodny przeciek między komórkami śródbłonka. (b) Schemat budowy BBB w kapilarze mózgowej: komórki śródbłonka ściśle połączone ze sobą, otoczone przez pericyty wbudowane w błonę podstawną oraz stopki astrocytów obejmujące naczynie. (c) Przykładowe strategie poprawy dostarczania leków do mózgu: podanie donosowe (spray do nosa), dołączanie ligandów (np. przeciwciał lub peptydów) do nanonośników w celu ukierunkowania na receptory BBB, powlekanie nanocząstek biomembranami (np. z błon komórkowych) maskujące je przed układem immunologicznym, oraz czasowe zaburzenie integralności BBB (np. ultradźwięki z mikro-pęcherzykami). (d) Różnorodne materiały stosowane w systemach nanonośnikowych: nanocząstki organiczne (np. liposomy, polymery, dendrymery, hydrożele), nieorganiczne (np. złoto, krzemionka, nanorurki węglowe) oraz biologiczne (np. egzosomy, bakterie) wykorzystywane do dostarczania leków do OUN.
Przykłady leków przenikających BBB w chorobach neurodegeneracyjnych
Choroba Alzheimera (AD): Jest to postępujące schorzenie neurodegeneracyjne cechujące się odkładaniem w mózgu płytek β-amyloidowych i splątków neurofibrylarnych tau, prowadzące do otępienia. Klasyczne leki stosowane w AD – inhibitory acetylocholinoesterazy (AChE) jak donepezil, rywastygmina, galantamina – zostały zaprojektowane jako małe, lipofilne związki, aby swobodnie przekraczać BBB na drodze dyfuzji. Donepezil (Mr ~380 Da) przenika względnie łatwo dzięki wysokiej lipofilowości (logP ~3) i niskiej masie, osiągając w płynie mózgowo-rdzeniowym stężenia skuteczne klinicznie. Wykazano, że w modelach zwierzęcych około 7–10% dawki donepezilu dociera do mózgu, co przy codziennym dawkowaniu daje działanie terapeutyczne. Niemniej, obecność P-gp ogranicza ten odsetek – blokowanie P-gp powoduje istotny wzrost stężenia donepezilu w OUN. Rywastygmina (Mr ~250 Da) jest bardziej hydrofilowa, ale jako prolek (karbaminian) ulega aktywacji w mózgu; dostępna jest nawet w formie systemu transdermalnego, skąd stopniowo przenika do krwi i dalej przez BBB. Galantamina (Mr ~287 Da) to alkaloid przenikający BBB również głównie na drodze dyfuzji biernej – jego skuteczność zależy od utrzymania odpowiedniego stężenia w osoczu, ponieważ szybko dyfunduje do OUN i równie szybko jest metabolizowana. Memantyna (antagonista NMDA, Mr ~180 Da) jest niewielką cząsteczką o umiarkowanej lipofilowości, przenikającą do mózgu na zasadzie dyfuzji – jej działanie polega na modylowaniu sygnalizacji glutaminergicznej w AD. Warto wspomnieć, że w AD trwają próby leczenia biologicznymi lekami celującymi w patologiczne białka – przeciwciała monoklonalne aducanumab, lecanemab, donanemab skierowane przeciw β-amyloidowi. Są to duże białka (~150 kDa) podawane dożylnie; jedynie <0,5% ich dawki przenika spontanicznie przez BBB (prawdopodobnie dzięki fizjologicznemu transportowi receptora FcRn oraz częściowo przez regiony z uszkodzoną barierą). Mimo to, jak wykazano w badaniach klinicznych, taka ilość wystarcza do związania i eliminacji amyloidu w mózgu – musi być jednak uzupełniona wysokimi dawkami i częstymi infuzjami. W celu zwiększenia tego odsetka opracowywane są przeciwciała bispecyficzne (np. wspomniane brain shuttle wykorzystujące anty-TfR). Na etapie badań jest także podanie donosowe przeciwciał anty-amyloidowych lub fragmentów tych przeciwciał, co potencjalnie mogłoby ominąć BBB i deponować lek w OUN przez nabłonek węchowy.
Choroba Parkinsona (PD): W PD dochodzi do zaniku neuronów dopaminergicznych istoty czarnej, skutkującego niedoborem dopaminy w prążkowiu i objawami ruchowymi. Sama dopamina nie przenika przez BBB (jest zbyt polarna i aktywnie usuwana), dlatego złotym standardem jest podawanie jej prekursora L-DOPA (lewodopy). Lewodopa, dzięki strukturalnemu podobieństwu do aminokwasu L-tyrozyny, jest transportowana przez nośnik LAT1 do mózgu. W celu zwiększenia jej dostępności centralnej łączy się ją z inhibitorami dekarboksylazy (karbidopa, benserazyd), które nie przenikają przez BBB – hamują one konwersję L-DOPY do dopaminy na obwodzie, nie wpływając na sam mózg. W rezultacie większa część dawki lewodopy dociera do OUN i tam ulega przemianie do dopaminy (w mózgu dekarboksylaza działa swobodnie, bo inhibitory nie przekraczają bariery). Inną kategorią leków w PD są agonisty receptorów dopaminowych (np. pramipeksol, ropinirol, rotigotyna) – są to stosunkowo małe cząsteczki o charakterze lipofilowym, dlatego przenikają BBB biernie. Pramipeksol (Mr ~211 Da) i ropinirol (Mr ~260 Da) osiągają w mózgu znaczące stężenia po podaniu doustnym, choć oba są substratami P-gp, co nieco ogranicza ich penetrację (mutacje w ABCB1 mogą wpływać na ich działanie kliniczne). Rotigotyna (Mr ~315 Da) ze względu na lipofilowość jest podawana w plastrach transdermalnych – lek uwalnia się powoli do krwi, skąd dyfunduje do mózgu (forma transdermalna omija efekt pierwszego przejścia i utrzymuje stałe stężenie sprzyjające penetracji). W PD stosuje się również inhibitory MAO-B (selegilina, rasagilina) – te aminy (Mr ~187–->267 Da) są bardzo lipofilowe, dzięki czemu łatwo przekraczają BBB i hamują rozkład dopaminy w samym mózgu. Co ciekawe, selegilina w dużych dawkach działa też jako donor fenyloetylaminy, co może ułatwiać jej transport (fenyloetyloamina jest endogenną cząsteczką sygnałową przechodzącą przez BBB). W zaawansowanej chorobie Parkinsona eksperymentuje się z podawaniem terapii białkowych (np. czynnika neurotroficznego GDNF) – te jednak nie przekroczą BBB, stąd próby bezpośrednich infuzji do mózgu lub wektorów wirusowych wprowadzanych chirurgicznie (ominiecie bariery). Rozważa się także zastosowanie skupionych ultradźwięków do poprawy dostarczania enzymatycznych terapii wymiany (np. enzymów zastępujących niedobory metaboliczne w rzadkich parkinsonizmach) – technologia ta jest we wczesnym stadium testów.
Stwardnienie zanikowe boczne (SLA): SLA charakteryzuje się degeneracją neuronów ruchowych i postępującym paraliżem. Riluzol – jedyny doustny lek modyfikujący przebieg SLA – jest małą cząsteczką (Mr ~234 Da) o umiarkowanej lipofilowości, która przenika przez BBB na drodze dyfuzji, ale w dość ograniczonym stopniu. Szacuje się, że biodostępność mózgowa riluzolu jest niska z powodu aktywności transporterów efluksowych; w modelach mysich zahamowanie P-gp i BCRP potęgowało stężenie riluzolu w OUN ponad dwukrotnie. To może częściowo tłumaczyć jego umiarkowaną skuteczność – obecnie trwają badania nad połączeniem riluzolu z inhibitorami P-gp, a także nad nowymi analogami o lepszej przenikalności. Edarawon (edaravone), lek o działaniu antyoksydacyjnym stosowany w SLA (i udarach), podawany jest dożylnie – jest stosunkowo niewielki (Mr ~253 Da) i przenika do mózgu, choć również jest substratem P-gp. Wprowadzono go do terapii SLA w Japonii i USA, jednak jego skuteczność zależy od wczesnego podania i być może od zdolności dotarcia do kluczowych obszarów rdzenia przedłużonego. Ponieważ riluzol i edarawon dają ograniczone efekty, intensywnie rozwija się nowe podejścia, np. terapie genowe i RNA. Oligonukleotydy antysensowne (ASO) skierowane przeciw zmutowanym genom (jak tofersen dla mutacji SOD1 w SLA) stanowią przełom – niestety, nie przekraczają BBB po podaniu obwodowym ze względu na duży rozmiar i polarny charakter. Dlatego tofersen i inne ASO podaje się bezpośrednio dokanałowo (do płynu mózgowo-rdzeniowego) poprzez punkcję lędźwiową, co omija barierę krew–mózg. Dostarczenie leku inwazyjnie do OUN zapewnia jego wysokie lokalne stężenie, ale wiąże się z ryzykiem powikłań procedury i nierównomiernym rozprowadzeniem w tkance nerwowej. Trwają zatem poszukiwania systemów nośnikowych, które pozwoliłyby przenieść terapie genowe do mózgu po podaniu dożylnym – testuje się np. wektory wirusowe AAV9 zmodyfikowane pod kątem tropizmu do OUN oraz nanocząstki lipidowe (LNP) dostarczające mRNA*. Co ciekawe, AAV9 podany do krwi u niemowląt potrafi przekroczyć BBB w stopniu terapeutycznym (zastosowano to w leczeniu rdzeniowego zaniku mięśni – terapii Zolgensma), jednak u dorosłych bariera jest mniej przepuszczalna dla wirusów. W SLA eksperymentalnie zastosowano też skupione ultradźwięki, aby zwiększyć penetrację leku do rdzenia kręgowego – w 2023 r. opublikowano pierwsze wyniki wskazujące na bezpieczeństwo tej metody i przejściowe otwarcie bariery krew-rdzeń dla terapii farmakologicznych.
Powyższe przykłady ilustrują, że każda klasa leków musi radzić sobie z barierą krew–mózg w odmienny sposób. Tabela 1 porównuje wybrane leki i technologie pod kątem mechanizmów pokonywania BBB oraz ich zastosowań.
Tabela 1. Porównanie wybranych leków stosowanych w OUN i strategii przenikania przez BBB.
| Lek lub technologia | Mechanizm pokonania BBB | Przykład / zastosowanie |
|---|---|---|
| Mała cząsteczka lipofilna | Bierna dyfuzja transkomórkowa przez śródbłonek; niska masa (< 400–500 Da) i wysoka rozpuszczalność w lipidach warunkują przenikanie przez barierę. Możliwy ograniczony efluks przez P-gp. | Donepezil (inhibitor AChE w chorobie Alzheimera, Mr 379 Da) – przenika BBB swobodnie dzięki lipofilowości, ale jest częściowo usuwany przez glikoproteinę P, co wpływa na jego stężenie w mózgu. |
| Prolek aktywowany w OUN | Chemiczna modyfikacja poprawia przepuszczalność, następnie enzymatyczna konwersja do formy aktywnej już w mózgu. | Rywastygmina (choroba Alzheimera) – jako karbaminian ulega aktywacji dopiero po przeniknięciu do mózgu; forma transdermalna zapewnia powolne uwalnianie i stały dopływ leku przez BBB. |
| Wykorzystanie transportera (LAT1) | Strukturalne upodobnienie do naturalnego substratu transportera obecnego na BBB, co umożliwia aktywny transport przez śródbłonek. | Levodopa (prekursor dopaminy w chorobie Parkinsona) – transportowana przez transporter aminokwasów LAT1 do OUN. Podawana z inhibitorem karboksylazy (karbidopa) dla zwiększenia dostępności mózgowej. |
| Nośnik nanocząsteczkowy z ligandem | Nanonośnik (np. liposom, nanoparticle polimerowy) wyposażony w ligand rozpoznawany przez receptor na BBB (np. transferrynę, apolipoproteinę, peptyd Angiopep). Ligand indukuje transcytozę receptorową i przenosi związany z nim nośnik wraz z lekiem przez barierę. | PEGylowane liposomy z glutationem – wykorzystują transporter glutationu na BBB, zwiększając dostarczanie leku do mózgu (badane w modelach choroby Alzheimera). Nanocząstki z transferryną – testowane w terapiach guzów mózgu (wiązanie TfR na śródbłonku, transport do wnętrza). |
| Nanoprzeciwciało / przeciwciało bispecyficzne | Single-domain antibody (~15 kDa) lub konstrukcja dwudomenowa: jedna domena wiąże receptor na BBB (np. TfR, receptor insulinowy), ułatwiając transcytozę, druga domena to część terapeutyczna (przeciwciało właściwe lub enzym). Mały rozmiar nanoprzeciwciała sprzyja także penetracji w głąb tkanki mózgowej. | Bispecyficzne przeciwciało anty-Aβ z domeną anty-TfR (tzw. Brain Shuttle) – w badaniach zwiększa dostarczanie leku w chorobie Alzheimera, przekraczając BBB dzięki interakcji z receptorem transferynowym. Nanoprzeciwciało przeciw tau – testowane w modelach AD; jego mała cząsteczka osiąga wyższe stężenia w mózgu niż pełne IgG, ale wymaga częstszego dawkowania z uwagi na krótki półokres. |
| Droga donosowa (intranazalna) | Podanie leku w postaci aerozolu do jamy nosowej – wykorzystanie transportu wzdłuż nerwu węchowego i trójdzielnego bezpośrednio do mózgu, z pominięciem BBB. | Donosowa insulina – badana strategia poprawy funkcji poznawczych w łagodnych zaburzeniach poznawczych i chorobie Alzheimera; insulina dociera do OUN szlakiem nerwowym, co może regulować metabolizm mózgowy. Donosowe podanie neuropeptydów (np. oksytocyny) – testowane w zaburzeniach autystycznych, pozwala ominąć barierę krew–mózg i szybko wywołać efekt centralny. |
| Czasowe otwarcie BBB (FUS) | Fizyczne, odwracalne rozszczelnienie połączeń ścisłych BBB na wybranym obszarze za pomocą skupionych ultradźwięków (FUS) w obecności mikro-pęcherzyków kontrastowych. Powstające siły mechaniczne na śródbłonku zwiększają przepuszczalność na kilkadziesiąt minut. | Ultradźwięki + przeciwciało monoklonalne – w badaniu klinicznym u pacjentów z chorobą Alzheimera zastosowanie FUS nad korą czołową ułatwiło przenikanie przeciwciała anty-amyloidowego do mózgu, co skutkowało redukcją złogów amyloidu (bez trwałego uszkodzenia BBB). FUS w SLA – badania (I fazy) wykazały bezpieczeństwo otwarcia BBB nad korą ruchową celem poprawy dostarczania leków neuroprotekcyjnych u chorych na SLA. |
| Egzosomowe nośniki leku | Wykorzystanie egzosomów – naturalnych pęcherzyków wydzielanych przez komórki – jako nanonośników zdolnych do fuzji z komórkami BBB. Egzosomy mogą przenosić leki (np. małe cząsteczki, siRNA) i dzięki swoim właściwościom przechodzić przez barierę oraz specyficznie kierować się do tkanek (np. do miejsc zapalnych). | Egzosomy neutrofilowe z lekiem przeciwnowotworowym – patent (CN114642736A) opisuje system, gdzie egzosomy z neutrofili przenoszą doksorubicynę przez BBB i kierują ją do guzów mózgu. W modelu glejaka u zwierząt uzyskano w ten sposób zwiększoną penetrację leku do guza i wydłużone przeżycie. Egzosomy inżynierowane (np. z komórek macierzystych) – badane pod kątem dostarczania siRNA w chorobie Alzheimera; dzięki receptorom adhezyjnym na powierzchni mogą przekraczać BBB i wprowadzać terapeutyczny ładunek do neuronów. |
Przegląd aktualnych patentów i nowych metod dostarczania leków do mózgu
Postęp w projektowaniu leków neuroaktywnych znajduje odzwierciedlenie w rosnącej liczbie patentów dotyczących pokonywania bariery krew–mózg. Poniżej przedstawiono wybrane najnowsze rozwiązania (po 2020 roku) wraz z przykładowymi zgłoszeniami patentowymi, które ilustrują kierunki rozwoju tej dziedziny:
- Platformy przeciwciał „shuttle”: Firmy biofarmaceutyczne opatentowały szereg technologii umożliwiających transport przeciwciał i białek terapeutycznych przez BBB. Przykładem jest platforma Brain Transporter firmy BioArctic – w 2022 r. uzyskano patent USA (US 11,498,974) na technologię ułatwiającą przenikanie bioterapeutyków przez barierę. Chociaż szczegóły techniczne nie zostały w pełni ujawnione, komunikat prasowy wskazuje, że technologia ta może polegać na modyfikacji przeciwciał (np. dodaniu domen wiążących receptor na BBB), co poprawia ich wychwyt przez śródbłonek i transcytozę do mózgu. Również Roche rozwija swój Brain Shuttle, oparty o przeciwciała bispecyficzne wiążące TfR – rozwiązania te są przedmiotem patentów międzynarodowych (np. WO2024208816, WO2023277627) i obejmują fuzyjne białka z domenami anty-TfR przyłączonymi do przeciwciał terapeutycznych. Celem jest uzyskanie przeciwciał o znacznie zwiększonej dystrybucji do mózgu, co pozwoli obniżyć dawki i poprawić skuteczność np. w terapii choroby Alzheimera (przeciwciała anty-Aβ) czy choroby Parkinsona (przeciwciała anty-α-synukleinowe).
- Nanonośniki z ukierunkowaniem na BBB: Kolekcja patentów dotyczy nanocząstek wyposażonych w ligandy zdolne do przekraczania BBB. Przykładowo, zgłoszenie US 2022175689 opisuje polimerowe nanocząstki z eksponowanymi na powierzchni ligandami (niekowalencyjnie związanymi) umożliwiającymi transport przez BBB. Ligandami tymi mogą być peptydy lub małe cząsteczki celujące w receptory BBB lub wykorzystujące szlaki transporterów. Innym przykładem jest europejski patent Arcticz EP3772001, opisujący nanonośniki z przeciwciałem anty-TfR i ich zastosowanie w dostarczaniu enzymów do OUN (terapie lizosomalnych chorób spichrzeniowych). Takie rozwiązania łączą stabilność i pojemność nanonośników (które mogą przenosić np. leki genowe, małe cząsteczki hydrofilowe) z mechanizmami aktywnego transportu przez barierę.
- Egzosomy i drug delivery biologiczny: Coraz więcej patentów skupia się na wykorzystaniu egzosomów lub innych pęcherzyków jako nośników. Wspomniany wcześniej patent CN114642736A to tylko jeden z przykładów – są też zgłoszenia dotyczące egzosomów modyfikowanych genetycznie, np. eksponujących na swojej powierzchni peptydy Penetratyny czy fragmenty przeciwciał, aby poprawić tropizm do mózgu. Ponadto opracowywane są syntetyczne egzosomy (protosomy) – nanokapsułki imitujące właściwości naturalnych egzosomów – i one również są zgłaszane do ochrony patentowej. Ten kierunek badań jest obiecujący ze względu na naturalną biokompatybilność i zdolność przenikania barier przez takie nośniki.
- Urządzenia i metody fizyczne: W zakresie metod otwierania BBB zgłoszono patenty na zogniskowane ultradźwięki z systemem sterowania MRI – np. US10874817 opisuje ulepszenia w koordynacji ultradźwięków z wstrzyknięciem mikro-bąbelków, zapewniające bezpieczne i powtarzalne otwarcie BBB. Inne zgłoszenia dotyczą implantowalnych urządzeń do lokalnego dostarczania leków (np. mikroinfuzory do ciągłego podawania leku do przestrzeni okołomózgowej czy wewnątrzmózgowo). Choć nie są to bezpośrednie metody przekraczania BBB w sensie farmakologicznym, patenty te pokazują wielokierunkowe podejście do problemu – od inwazyjnych bypassów po nieinwazyjne techniki neuromodulacyjne.
- Peptydy przenikające i chemiczne modyfikatory BBB: W literaturze patentowej pojawiają się również nowe sekwencje peptydów i białek fuzyjnych zdolnych do przenikania BBB. Jedno ze zgłoszeń (WO2023138107) dotyczy chimerycznego białka z domeną wiążącą LRP1 i neurotrofiną, które może przekraczać BBB i dostarczać czynnik wzrostu neuronów w chorobach neurodegeneracyjnych. Inne patenty opisują zastosowanie peptydów zwiększających przepuszczalność (inspirowanych toksynami czy białkami wirusowymi) jako adjuwantów poprawiających dystrybucję towarzyszących leków do mózgu. Przykładem jest analog bradykininy Cereport, który choć klinicznie nie spełnił pokładanych nadziei, doczekał się szeregu modyfikacji chronionych patentami, mających wydłużyć i ukierunkować jego działanie otwierające BBB lokalnie i kontrolowanie.
- Terapie genowe i mRNA dla OUN: W dobie medycyny RNA pojawiły się patenty na formulacje mRNA dostarczane do mózgu. Firma Moderna zgłosiła patenty dotyczące nanocząstek lipidowych (LNP) przenikających BBB, zawierających mRNA kodujące enzymy neuronowe czy czynniki neuroprotekcyjne. Jednym z rozwiązań jest powleczenie LNP polimerami lub przeciwciałami anty-TfR, aby skupić ich transport do mózgu. Chociaż większość tych technologii jest na wczesnym etapie, chronione są potencjalne zastosowania w leczeniu np. choroby Parkinsona (mRNA dla dekarboksylazy aromatycznych L-aminokwasów) czy choroby Alzheimera (mRNA dla enzymów degradujących amyloid).
Podsumowując, innowacje w zakresie dostarczania leków do OUN dynamicznie się rozwijają, łącząc wiedzę z biologii BBB, inżynierii biomateriałów i biologii molekularnej. Najnowsze badania po 2020 roku koncentrują się na hybrydowych strategiach, które są wielowymiarowe: np. połączenie nośnika nanotechnologicznego z elementem biologicznym (ligandem, przeciwciałem) oraz zastosowaniem zewnętrznego bodźca (ultradźwięków, pola magnetycznego) dla uzyskania maksymalnego efektu. Wyzwania pozostają – szczególnie kwestia bezpieczeństwa (czy długotrwałe manipulacje BBB nie wywołają skutków ubocznych) oraz efektywności translacji tych metod na grunt kliniczny. Niemniej, rosnąca liczba patentów i publikacji wskazuje, że jesteśmy świadkami nowej ery w projektowaniu leków neuroaktywnych. Bariery, które niegdyś były uznawane za nieprzekraczalne, dziś są stopniowo pokonywane dzięki pomysłowości naukowców i multidyscyplinarnemu podejściu. Można oczekiwać, że w nadchodzących latach doczekamy się przełomowych terapii chorób OUN, w których dawny wroga – barierę krew–mózg – obrócono na swoją korzyść, czyniąc z niej sojusznika w precyzyjnym dostarczaniu leków do najbardziej wrażliwego z organów, jakim jest ludzki mózg.
Bibliografia:
- Wu, D. i in. (2023). The blood–brain barrier: Structure, regulation and drug delivery. Signal Transduction and Targeted Therapy, 8(217).
- Teleanu, R.I. i in. (2022). Current Strategies to Enhance Delivery of Drugs across the Blood–Brain Barrier. Pharmaceutics, 14(5), 987.
- Zheng, F. i in. (2022). Applications of nanobodies in brain diseases. Frontiers in Immunology, 13:978513.
- Frontiers in Drug Delivery (2025). Strategies for delivering drugs across the blood–brain barrier for the treatment of neurodegenerative diseases.
- Jablonski, M.R. i in. (2019). Blood-Brain Barrier Driven Pharmacoresistance in ALS. Pharmacology & Therapeutics, 199, 117-130.
- BioArctic AB (2022). Press release: New patent in the US for blood-brain barrier transport technology.
- Google Patents WO2023277627A1 (2023). Blood-brain barrier permeable fusion protein.
- Google Patents CN114642736A (2022). Neutrophil exosome drug delivery system for blood-brain barrier crossing.
- Spieler, D. i in. (2020). Donepezil is actively transported out of the brain by P-glycoprotein in mice. Journal of Psychiatric Research, 128, 33-39.
- Shen, J. i in. (2023). Intranasal delivery as a strategy for bypassing the blood–brain barrier: recent advances and future perspectives. (Review)
- Chen, Y. i in. (2021). Focused ultrasound-enhanced BBB permeability in Alzheimer’s disease models. Journal of Controlled Release, 330, 38-49.
Opracowanie: Rafał Klasiński / Fundacja Independent Institute of Chemical Processes.