Streszczenie wykonawcze
Narastające dowody wskazują, że neurozapalanie (utrwalona, nieprawidłowo regulowana odpowiedź immunologiczna ośrodkowego układu nerwowego) nie jest wyłącznie „towarzyszem” neurodegeneracji, lecz współtworzy środowisko sprzyjające uszkodzeniu synaps i neuronów, nasileniu patologii białkowych oraz dysfunkcji bariery krew–mózg. Kluczowe elementy tej reakcji obejmują aktywację mikrogleju i astrocytów, wydzielanie cytokin i chemokin oraz rekrutację komórek odpornościowych z obwodu w warunkach uszkodzenia BBB (Ransohoff, 2016; Shi i in., 2025).
Na poziomie molekularnym centralne znaczenie mają szlaki rozpoznawania wzorców zagrożenia (np. TLR), transdukcji sygnału prozapalnego (NF-κB), aktywacji inflamasomu (NLRP3) oraz układu dopełniacza (complement). Te mechanizmy mogą początkowo pełnić funkcje ochronne (usuwanie agregatów białkowych, wsparcie naprawy), lecz w przewlekłej fazie sprzyjają samonapędzającemu się cyklowi „zapalenie–degeneracja” (Heneka i in., 2015; Zhang i in., 2023).
W chorobie Alzheimera (AD) immunogenetyka (badania GWAS) konsekwentnie wskazuje na udział szlaków mikroglejowych i odporności w ryzyku choroby, co wzmacnia koncepcję, że neurozapalanie jest elementem patogenezy, a nie wyłącznie odpowiedzią wtórną (Bellenguez i in., 2022; Kunkle i in., 2019).
W chorobie Parkinsona (PD) i ALS obserwuje się zarówno sygnały centralnej aktywacji glialnej, jak i odchylenia profili cytokin we krwi i/lub płynie mózgowo-rdzeniowym (Qin i in., 2016; Hu i in., 2017).
Kluczowe wyzwanie translacyjne pozostaje niezmienne: liczne interwencje o szerokim profilu przeciwzapalnym nie wykazały skuteczności klinicznej w zaawansowanych stadiach chorób (np. próby prewencji AD z NLPZ; próby repurposingu minocykliny), a nowsze strategie immunomodulacji mikrogleju mogą wykazywać wyraźne efekty farmakodynamiczne bez przełożenia na punkt końcowy kliniczny (ADAPT; Mummery i in., 2026).
W praktyce klinicznej rośnie rola biomarkerów glialnych (np. GFAP, sTREM2, YKL-40/CHI3L1) oraz obrazowania TSPO-PET jako narzędzi stratyfikacji i monitorowania, ale heterogeniczność wyników (wpływ współchorobowości, różnice metod oznaczeń) ogranicza ich uniwersalne zastosowanie (Brosseron i in., 2018; De Picker i in., 2023; Kim i in., 2023).
Poziom dowodów (dla tezy głównej): wysoki dla współwystępowania i znaczenia neurozapalania w neurodegeneracji (neuropatologia, genetyka, biomarkery; dowody epidemiologiczne/kliniczne) oraz wysoki dla mechanizmów przyczynowych w modelach (dowody eksperymentalne), umiarkowany dla skutecznych terapii modyfikujących neurozapalanie w AD/PD/ALS (dowody z badań klinicznych często negatywne lub niespójne).
Wstęp
Pojęcie „stanu zapalnego mózgu” przez lata bywało traktowane jako opisowa etykieta zmian towarzyszących odkładaniu patologicznych białek. Obecnie termin neurozapalanie odnosi się do szerokiego spektrum procesów, w których komórki OUN (mikroglej, astrocyty, komórki śródbłonka, perycyty) oraz – w określonych warunkach – komórki odpornościowe z krwi wspólnie kształtują środowisko determinujące przeżycie neuronów, stan synaps i przebieg regeneracji (Ransohoff, 2016; Shi i in., 2025).
Kluczowa zmiana paradygmatu polega na przejściu od pytania „czy w neurodegeneracji występuje zapalenie?” do pytania „kiedy, w jakiej fazie i w jakim fenotypie odpowiedź odpornościowa OUN jest adaptacyjna, a kiedy staje się czynnikiem uszkadzającym?”. To rozróżnienie wynika m.in. z danych o heterogenności mikrogleju (różne programy transkrypcyjne w zależności od etapu choroby i lokalizacji) oraz o toksycznych podtypach astrocytów indukowanych przez sygnały mikroglejowe (Krasemann i in., 2017; Liddelow i in., 2017).
W AD, PD i ALS neurozapalanie jest rozważane jako element wspólny: agregaty białkowe (Aβ/tau w AD, α-synukleina w PD, m.in. białka związane z ALS) mogą aktywować receptory rozpoznające wzorce zagrożenia (PRR), uruchamiając kaskady NF-κB, TLR i NLRP3 oraz modulując dopełniacz. W przewlekłej fazie może to prowadzić do błędnego „tagowania” synaps do eliminacji, wzmożonego stresu oksydacyjnego, zaburzeń mitochondrialnych i dysfunkcji BBB – czyli do zjawisk, które przyspieszają degenerację sieci neuronalnych (Heneka i in., 2015; Zhang i in., 2023).
Cel artykułu: krytyczny przegląd definicji neurozapalania, mechanizmów komórkowych i molekularnych, dowodów epidemiologicznych i eksperymentalnych łączących zapalenie z AD/PD/ALS (oraz wybranymi innymi chorobami), oraz analiza biomarkerów i interwencji (farmakologicznych, immunomodulacyjnych i stylu życia), z identyfikacją luk w wiedzy.
Metody
Przegląd ma charakter narracyjny, z elementami selekcji typowymi dla przeglądu ukierunkowanego na dowody wysokiej jakości. Dobór literatury obejmował publikacje recenzowane oraz źródła rejestrowe dotyczące badań klinicznych.
Zakres wyszukiwania obejmował prace opublikowane głównie w latach 2010–2026 (z uwzględnieniem klasycznych prac mechanistycznych starszych, jeśli stanowią kamienie milowe). Preferowano przeglądy systematyczne i metaanalizy, badania randomizowane, duże kohorty i badania genetyczne GWAS, a także prace mechanistyczne w modelach zwierzęcych i komórkowych. Jako główne źródła włączano publikacje anglojęzyczne (dominujące w neuroimmunologii i neurologii) oraz – jeśli dostępne i recenzowane – publikacje polskojęzyczne (np. prace przeglądowe o komórkach glejowych).
Używano kombinacji słów kluczowych (polskich i angielskich) obejmujących m.in.: neuroinflammation/neurozapalanie, microglia/mikroglej, astrocytes/astrocyty, blood–brain barrier/BBB, NF-κB, NLRP3 inflammasome, toll-like receptors/TLR, complement, biomarkers/CSF/plasma, Alzheimer’s/Parkinson’s/ALS, clinical trial/randomized, meta-analysis/systematic review. W części klinicznej priorytetowo traktowano prace raportujące wyniki badań randomizowanych (np. ADAPT, próba TREM2-agonisty AL002) oraz metaanalizy biomarkerów.
Wykluczono źródła nierecenzowane (preprinty) jako podstawa wnioskowania, a także doniesienia popularnonaukowe i materiały marketingowe. Jeśli przywoływano hipotezy lub wnioski o charakterze interpretacyjnym, zaznaczano to wprost oraz opierano na źródłach przeglądowych.
Wyniki i omówienie
Definicja neurozapalania i jego „dwoista natura”
Neurozapalanie można ująć jako zespół procesów nieautonomicznych względem neuronu, które – poprzez komórki wspierające (glej), naczynia i elementy odporności – determinują uszkodzenie, dysfunkcję lub powrót do homeostazy w OUN. Takie ujęcie podkreśla, że nie chodzi wyłącznie o „obecność komórek odpornościowych”, lecz o zmianę warunków środowiskowych neuronu, w tym sygnalizacji cytokinowej, metabolizmu, funkcji synaps i integralności BBB (Ransohoff, 2016; Shi i in., 2025).
Kluczowe jest rozróżnienie neurozapalania ostrego i kontrolowanego (np. po urazie, infekcji – zwykle z celem eliminacji czynnika i naprawy) od neurozapalania przewlekłego, „niskiego stopnia”, utrwalonego. To drugie częściej koreluje z neurodegeneracją i bywa traktowane jako element „inflammaging” (starzenie się z komponentą prozapalną) oraz „zapalnego napędu” patologii białkowych i synaptycznych (Lassmann, 2022; Zhang i in., 2023).
W literaturze rośnie krytyka nadużywania terminu neurozapalanie jako synonimu samej aktywacji gleju. Koncepcje nowsze akcentują wielowarstwowość odpowiedzi: od wrodzonej odporności mózgu (mikroglej, dopełniacz), przez odporność nabytą (limfocyty), po „osiowe” powiązania obwód–mózg (systemowy stan zapalny jako modulator przebiegu choroby) (Galea i in., 2023; Shi i in., 2025).
Poziom dowodów: wysoki dla obecności i biologicznej istotności neurozapalania w neurodegeneracji (przeglądy, neuropatologia, biomarkery), umiarkowany dla precyzyjnego rozdzielenia przyczynowości w człowieku (często współwystępowanie i sprzężenia zwrotne).
Mechanizmy komórkowe
Mikroglej to rezydentne makrofagi OUN pełniące w fizjologii funkcje nadzoru, fagocytozy i „przycinania” synaps podczas rozwoju. W neurodegeneracji mikroglej może przechodzić w stany aktywacji o odmiennych programach transkrypcyjnych – od fenotypów wspierających usuwanie złogów po fenotypy nasilające neurotoksyczne mediatory i dysfunkcję synaptyczną (Gao i in., 2023; Deczkowska i in., 2018).
Badania single-cell w modelach AD opisały tzw. disease-associated microglia (DAM) – populacje mikrogleju związane z obszarami neurodegeneracji i patologią Aβ, z programem aktywowanym etapowo i częściowo zależnym od TREM2. W interpretacji funkcjonalnej DAM bywa rozważany jako próba adaptacyjnego „ograniczenia” uszkodzeń, choć w przewlekłej fazie może współtworzyć środowisko prozapalne (Keren-Shaul i in., 2017; Deczkowska i in., 2018).
Astrocyty są kluczowe dla homeostazy synaptycznej (buforowanie K⁺, metabolizm glutaminianu, wsparcie energetyczne neuronów, udział w BBB). W warunkach patologii mogą jednak przechodzić w stany reaktywne, w tym opisywane jako neurotoksyczne. Praca Liddelow i in. wykazała, że mikroglej może indukować specyficzny, neurotoksyczny program reaktywnych astrocytów poprzez sygnały IL-1α, TNF oraz C1q (Liddelow i in., 2017). Ten mechanizm łączy komórki wrodzonej odporności (mikroglej), cytokiny oraz dopełniacz w jeden układ „przełączników” neurotoksyczności (Liddelow i in., 2017).
Cytokiny i chemokiny są językiem komunikacji zapalnej. W neurodegeneracji często omawia się podwyższenia lub zmiany osi IL-1β/IL-18 (często powiązanej z inflamasomem), IL-6, TNF-α oraz chemokin rekrutujących monocyty (np. MCP-1/CCL2). Metaanalizy wskazują na istotne, ale heterogeniczne odchylenia tych mediatorów w AD, PD i ALS – co sugeruje, że nie istnieje pojedynczy „uniwersalny” profil cytokinowy, a wyniki silnie zależą od fazy choroby, współchorobowości i metod oznaczania (Swardfager i in., 2010; Qin i in., 2016; Hu i in., 2017).
Bariera krew–mózg (BBB) stanowi funkcjonalny interfejs między odpornością obwodową a OUN. Jej dysfunkcja może umożliwiać przenikanie mediatorów zapalnych oraz niektórych populacji komórek odpornościowych, wzmacniając neurozapalanie i tworząc pętlę sprzężenia zwrotnego. Przeglądy BBB w AD podkreślają udział komórek śródbłonka, perycytów i stóp końcowych astrocytów w utrzymaniu szczelności oraz w immunologicznej „kuracji” transportu (Alkhalifa i in., 2023). W ujęciu biomarkerowym uszkodzenie perycytów bywa śledzone przez markery takie jak sPDGFRβ w płynie mózgowo-rdzeniowym (Miners i in., 2019; Sweeney i in., 2020).
Rola komórek odporności obwodowej (monocyty, limfocyty) w chorobach neurodegeneracyjnych jest złożona: od ewentualnej rekrutacji i prezentacji antygenów po modulację fenotypu mikrogleju. Ujęcia przekrojowe neurozapalania podkreślają, że „odporność mózgu” obejmuje zarówno komponenty wewnątrz-OUN, jak i w określonych warunkach komponenty infiltrujące (Shi i in., 2025; Ransohoff, 2016).
Poziom dowodów: wysoki dla roli mikrogleju/astrocytów w modelach i neuropatologii; umiarkowany–wysoki dla znaczenia BBB w AD; umiarkowany dla specyficznych mechanizmów infiltracji komórek odpornościowych w AD/PD/ALS w człowieku (często zależne od modeli i technik).
Szlaki molekularne: NF-κB, NLRP3, TLR i dopełniacz
NF-κB jest jednym z głównych regulatorów transkrypcji genów prozapalnych w komórkach glejowych. Aktywacja NF-κB w mikrogleju i astrocytach może promować produkcję cytokin, enzymów prozapalnych oraz mediatorów stresu oksydacyjnego, wspierając utrwalenie stanu zapalnego w OUN (Shabab i in., 2017; Biswas i in., 2023). W praktyce NF-κB działa również jako element „primingu” dla inflamasomu – zwiększa ekspresję komponentów NLRP3 i pro–IL-1β (Shin i in., 2026).
TLR (Toll-like receptors) są receptorami rozpoznającymi PAMP/DAMP i w OUN szczególnie istotne są TLR na mikrogleju i astrocytach. Mogą być aktywowane przez patogeny, ale także przez endogenne sygnały uszkodzenia oraz – w kontekście AD – przez agregaty białkowe i produkty ich degradacji. Aktywacja TLR uruchamia kaskady sygnałowe (często przez adaptor MyD88/TRIF), prowadząc do aktywacji NF-κB i wytwarzania mediatorów zapalnych (Squillace i in., 2022; Dabi i in., 2023). Prace przeglądowe dotyczące mikroglejowych TLR w AD podkreślają, że niektóre sygnały TLR mogą mieć komponent ochronny (ułatwienie fagocytozy Aβ) we wczesnych fazach, przy jednoczesnym ryzyku utrwalenia prozapalnego fenotypu w fazie przewlekłej (Su i in., 2016; Squillace i in., 2022).
Inflamasom NLRP3 to wielobiałkowy kompleks aktywujący kaspazę-1 i dojrzewanie IL-1β oraz IL-18. Klasyczny model aktywacji obejmuje dwa etapy: sygnał 1 („priming”) – często przez TLR/NF-κB – oraz sygnał 2 („activation”) indukowany m.in. przez stres komórkowy, zaburzenia jonowe, ROS czy cząstki krystaliczne; te zasady są szczegółowo omawiane w aktualnych przeglądach mechanistycznych (Shin i in., 2026; Blevins i in., 2022).
W AD praca Heneka i in. wykazała w modelu APP/PS1, że brak NLRP3 lub kaspazy-1 wiąże się z ochroną funkcji poznawczych, obniżeniem aktywacji IL-1β i zwiększeniem klirensu Aβ, co stanowi silny argument eksperymentalny, że oś NLRP3/kaspaza-1 może być czynnikiem sprawczym w kaskadzie patologicznej (Heneka i in., 2013). Analogicznie, w PD i innych chorobach neurodegeneracyjnych NLRP3 bywa wiązany z neurozapalaniem i dysfunkcją mitochondrialną, choć podstawy przyczynowe u człowieka pozostają trudniejsze do udowodnienia (Han i in., 2023; Holbrook i in., 2021).
Układ dopełniacza (complement) w OUN pełni role homeostatyczne (m.in. w fizjologicznej eliminacji synaps podczas rozwoju), ale w neurodegeneracji może zostać patologicznie reaktywowany. Koncepcja „tagowania” synaps przez składowe dopełniacza (np. C1q/C3) i następczej eliminacji przez mikroglej (receptory dopełniacza) jest jednym z najlepiej udokumentowanych mechanizmów łączących odporność wrodzoną z utratą synaps (Hong i in., 2016; Batista i in., 2024).
Współczesne przeglądy dopełniacza w AD omawiają także oś C5a–C5aR1 jako napędzającą polaryzację glialną i stan zapalny, a badania przedkliniczne z antagonistą C5aR1 (np. PMX205) wskazują na możliwość poprawy funkcji poznawczych i ograniczenia szkodliwej aktywacji gleju w modelach mysich, przy jednoczesnym zachowaniu elementów odpowiedzi ochronnej (Schartz i in., 2024; Papavergi i in., 2025). To stanowi ważny sygnał, że „wyciszanie” dopełniacza może wymagać precyzyjnego doboru etapu choroby i celu molekularnego (Schartz i in., 2024; Zelek i in., 2025).
Poziom dowodów: wysoki dla roli NF-κB/TLR/NLRP3/dopełniacza jako osi mechanistycznych w neurozapalaniu (modele i biologia układu odporności); wysoki dla przyczynowej roli NLRP3 w modelach AD; umiarkowany dla skutecznego i bezpiecznego „trafienia” tych osi u ludzi (dowody kliniczne ograniczone).
Dowody łączące neurozapalanie z AD, PD, ALS i innymi chorobami
Choroba Alzheimera (AD). Dowody wspierające oś neurozapalną w AD pochodzą z trzech głównych obszarów: (1) immunogenetyki, (2) neuropatologii i mechanizmów w modelach oraz (3) biomarkerów płynowych i obrazowych.
Po pierwsze, duże metaanalizy GWAS dla AD identyfikują loci związane z odpornością i funkcją mikrogleju, co wskazuje, że przynajmniej część ryzyka AD jest mediowana przez szlaki immunologiczne (Kunkle i in., 2019; Bellenguez i in., 2022). Jest to silny argument przeciwko uznawaniu zapalenia wyłącznie za epifenomen patologii amyloidowej (choć nie przesądza o kierunku w każdym przypadku) (Kunkle i in., 2019; Bellenguez i in., 2022).
Po drugie, przegląd Heneka i in. podsumowuje, że agregaty białkowe działają jak bodźce dla receptorów rozpoznających wzorce na mikrogleju i astrogleju, wyzwalając odpowiedź wrodzoną, której przewlekłe utrzymanie koreluje z progresją i ciężkością AD (Heneka i in., 2015). Eksperymentalnie, NLRP3/kaspaza-1 i dopełniacz są osiami, dla których wykazano przyczynowe znaczenie w modelach (Heneka i in., 2013; Hong i in., 2016).
Po trzecie, metaanalizy wykazują, że AD jest związana ze zmianami w stężeniach cytokin i markerów zapalnych w surowicy/osoczu, choć różnice są umiarkowane i obarczone heterogenicznością (Swardfager i in., 2010; Lai i in., 2017). Podobnie, część markerów glialnych w PMR (np. YKL-40/CHI3L1, sTREM2) wykazuje zależności stadialne i prognostyczne, co sugeruje, że można „zobaczyć” komponent zapalno-glialny w biomarkerach (Craig-Schapiro i in., 2010; Wang i in., 2024).
Choroba Parkinsona (PD). W PD obserwuje się zarówno dowody na aktywację mikrogleju (np. w badaniach przeglądowych i biomarkerowych), jak i zmiany profilu cytokin. Metaanaliza markerów zapalnych w PD wskazuje na odchylenia w stężeniach wybranych cytokin w porównaniu do kontroli, ale – podobnie jak w AD – problemem jest nieswoistość i wpływ zmiennych zakłócających (Qin i in., 2016).
Od strony epidemiologii, obserwacje dotyczące NLPZ i ryzyka PD są niespójne: niektóre badania sugerują związek ochronny (szczególnie dla ibuprofenu lub nieaspirynowych NLPZ), podczas gdy część metaanaliz wykazuje brak efektu lub efekt zależny od podgrup i jakości badań (Gao i in., 2011; Badawoud i in., 2024). Wnioski praktyczne są ostrożne: nawet jeśli istnieje efekt ochronny w części populacji, nie stanowi to podstawy do rekomendacji NLPZ jako prewencji PD z uwagi na ryzyko działań niepożądanych i niejednoznaczność danych (Gao i in., 2011; Badawoud i in., 2024).
Interesującym sygnałem epidemiologicznym są dane kohortowe sugerujące, że redukcja systemowego stanu zapalnego terapiami biologicznymi (np. anty-TNF w IBD) może wiązać się z niższą zapadalnością na PD (Peter i in., 2018; Potashman i in., 2025). Należy jednak podkreślić, że są to badania obserwacyjne: nawet przy korektach statystycznych pozostaje ryzyko resztkowego konfudowania, a związek nie dowodzi, że te same terapie będą skuteczne jako leczenie PD (Peter i in., 2018; Potashman i in., 2025).
Stwardnienie zanikowe boczne (ALS). W ALS neurozapalanie obejmuje aktywację mikrogleju i astrocytów w rdzeniu kręgowym oraz zmiany w profilach cytokin w surowicy i PMR. Metaanaliza wykazała podwyższone poziomy wybranych cytokin we krwi pacjentów z ALS, choć kierunek i wielkość efektów zależą od cytokiny oraz doboru badań (Hu i in., 2017). Aktualne przeglądy podkreślają złożoność roli mikrogleju: fenotypy ochronne i szkodliwe mogą współistnieć, a ich przewaga może zmieniać się w czasie choroby (Stacchiotti i in., 2025; „Microglia in ALS…”, 2025).
Inne choroby neurodegeneracyjne. Przeglądy mikrogleju w neurodegeneracji wskazują, że podobne motywy (aktywacja gleju, dopełniacz, sygnały DAMP/PAMP) pojawiają się również w otępieniu z ciałami Lewy’ego, otępieniach czołowo-skroniowych, Huntingtonie czy tauopatiach, choć mechanizmy inicjujące i dominujące ścieżki mogą się różnić (Gao i in., 2023). W praktyce oznacza to, że „neurozapalanie” jest wspólną platformą biologiczną, ale cele terapeutyczne muszą być dopasowane do biologicznego podtypu choroby i fazy (Gao i in., 2023; Lassmann, 2022).
Poziom dowodów: wysoki dla AD (genetyka + mechanizmy eksperymentalne + biomarkery), umiarkowany–wysoki dla PD i ALS (silne dane biomarkerowe/eksperymentalne, epidemiologia wspierająca, ale mniejsza przyczynowość w człowieku).
Biomarkery neurozapalania w PMR i krwi
Biomarkery neurozapalania można podzielić na: (1) markery reaktywności astrocytów i mikrogleju, (2) cytokiny/chemokiny, (3) markery dysfunkcji BBB i naczyniowe, (4) markery obrazowe (tu: TSPO-PET – choć nie jest biomarkerem płynowym, bywa kluczowy w badaniach translacyjnych).
W AD biomarkery glialne zyskują szczególne znaczenie, ponieważ mogą uzupełniać klasyczne markery Aβ/tau o informację o „odpowiedzi tkankowej” (glioza, aktywacja mikrogleju). Systematyczne przeglądy biomarkerów neurozapalnych podkreślają jednak, że standaryzacja i kliniczna użyteczność wciąż są w trakcie kształtowania (Heneka i in., 2025; Brosseron i in., 2018).
Tabela porównawcza biomarkerów neurozapalania
| Biomarker | Materiał | Co odzwierciedla biologicznie | Choroby z najsilniejszymi danymi | Przydatność diagnostyczna / prognostyczna | Ograniczenia i uwagi |
|---|---|---|---|---|---|
| GFAP (glial fibrillary acidic protein) | Krew (osocze) i PMR | Reaktywność/uszodzenie astrocytów (astrogliosis) | AD (kontinuum), także: PD z otępieniem | Metaanaliza wskazuje na potencjał GFAP jako biomarkera krwi w AD; badania longitudinalne sugerują wartość diagnostyczną i prognostyczną na wczesnych etapach | Nieswoisty dla AD (wzrasta też w innych uszkodzeniach OUN); zależny od metody oznaczeń i populacji (Kim i in., 2023; Montoliu-Gaya i in., 2023) |
| YKL-40 / CHI3L1 | PMR (i czasem krew) | Aktywacja glejowa, szczególnie astrocytów; remodeling i zapalenie | AD; także sygnały w innych NDD | Wzrost w AD; sugerowana wartość prognostyczna w stadiach przedklinicznych i we wczesnej chorobie | Heterogeniczność wyników; wpływ wieku i współchorobowości; raczej marker procesów towarzyszących niż swoisty test (Craig-Schapiro i in., 2010; Roveta i in., 2024) |
| sTREM2 (soluble TREM2) | PMR (krew mniej spójnie) | Aktywacja mikrogleju i sygnalizacja TREM2 | AD (MCI/AD), badania stadialne | Metaanalizy wskazują na podwyższenia sTREM2 w PMR w MCI/AD; możliwe powiązania z dynamiką choroby | Dane krwi niespójne; interpretacja zależna od etapu (aktywacja mikrogleju może być częściowo kompensacyjna) (Wang i in., 2024; Heneka i in., 2025) |
| Cytokiny (np. IL-6, TNF-α, IL-1β) | Krew i PMR | Oś prozapalna/odpornościowa; odpowiedź systemowa i centralna | AD, PD, ALS (metaanalizy) | W metaanalizach – różnice grupowe; potencjalnie korelacje z ciężkością | Bardzo ograniczona swoistość; duża zmienność; silny wpływ infekcji i chorób współistniejących (Swardfager i in., 2010; Qin i in., 2016; Hu i in., 2017) |
| CHIT1 (chitotriosidase) i chitynazy (np. CHI3L1) | PMR i krew | Aktywacja mikrogleju/makrofagów; komponent neurozapalny | ALS (najsilniej), także NDD | Metaanalizy wskazują na potencjał diagnostyczny chitynaz w ALS | Biomarkery pomocnicze; w ALS wciąż konkurują z markerami neurodegeneracji (np. NfL) (meta-analiza chitynaz w ALS, 2024) |
| TSPO-PET (obrazowanie) | PET | Marker aktywacji komórek glejowych (gł. mikrogleju) | Różne choroby OUN, w tym NDD | Metaanalizy TSPO-PET pokazują różnice między grupami i potencjał monitorowania odpowiedzi na terapię | Interpretacja zależna od ligandu i polimorfizmów TSPO; koszt i dostępność kliniczna (De Picker i in., 2023) |
| sPDGFRβ (marker perycytów) | PMR | Uszkodzenie perycytów i dysfunkcja BBB | AD i otępienia naczyniowe/ mieszane | Związki z markerami BBB i patologią AD; potencjał do fenotypowania komponenty naczyniowej | Wciąż biomarker w fazie walidacji; wymaga standaryzacji i interpretacji w kontekście BBB |
Wnioski z tabeli są praktyczne: najbardziej obiecujące biomarkery „zapalne” w neurodegeneracji to obecnie markery glialne (GFAP, YKL-40, sTREM2) i obrazowanie TSPO-PET, natomiast klasyczne cytokiny i CRP pozostają zbyt nieswoiste do diagnostyki różnicowej bez kontekstu klinicznego. Jednocześnie nawet biomarkery glialne mogą pełnić przede wszystkim rolę stratyfikacji (kto ma wysoki komponent glialny?) oraz monitorowania (czy terapia modulująca mikroglej zmienia sygnał?), a nie samodzielnej diagnozy nozologicznej (Brosseron i in., 2018; Heneka i in., 2025).
Poziom dowodów: wysoki dla GFAP/YKL-40/sTREM2 jako markerów różnic grupowych w AD (metaanalizy i badania longitudinalne), umiarkowany dla ich twardej wartości prognostycznej i decyzji terapeutycznych; umiarkowany dla ALS chitynaz jako markerów wspomagających; umiarkowany–wysoki dla TSPO-PET jako narzędzia badawczego (De Picker i in., 2023; Kim i in., 2023; Wang i in., 2024).
Interwencje: farmakologiczne, immunomodulacyjne i styl życia
Interwencje farmakologiczne o profilu przeciwzapalnym
Najbardziej klasyczna hipoteza terapeutyczna zakładała, że hamowanie COX i redukcja prostaglandyn (NLPZ) mogą spowolnić lub zapobiec AD. Duże badania prewencyjne ADAPT nie potwierdziły jednak skuteczności naproksenu ani celekoksybu w prewencji otępienia ani w spowalnianiu spadku funkcji poznawczych; pojawiały się nawet sygnały możliwego efektu niekorzystnego dla części punktów końcowych (Lyketsos i in., 2007; Martin i in., 2008). Te wyniki stanowią ważną lekcję: szeroka immunosupresja lub niespecyficzne wyciszanie zapalenia nie musi trafiać w właściwy mechanizm, moment i miejsce w kaskadzie choroby (Lyketsos i in., 2007; Martin i in., 2008).
Repurposing minocykliny – antybiotyku z działaniem przeciwzapalnym i modulującym mikroglej w modelach – również nie przyniósł przełomu: randomizowana próba u osób z łagodną AD nie wykazała spowolnienia pogorszenia funkcji poznawczych ani funkcjonalnych w obserwacji 24 miesięcy, a wyższa dawka była gorzej tolerowana (Howard i in., 2019/2020). Dodatkowo w ALS minocyklina w badaniu fazy III okazała się nieskuteczna, a w analizach raportowano nawet szybsze pogarszanie w grupie leczonej (Gordon i in., 2007; Howard i in., 2019/2020).
Poziom dowodów: wysoki (RCT) dla braku klinicznej skuteczności NLPZ w prewencji AD w ADAPT oraz braku skuteczności minocykliny w łagodnej AD i w ALS.
Immunomodulacja ukierunkowana na mikroglej i szlaki immunologiczne
Nowsze podejście nie polega na „wygaszaniu zapalenia”, lecz na przesterowaniu programu odpornościowego OUN – np. przez modulację TREM2 (receptor ważny dla fagocytozy i fenotypu mikrogleju). Próba kliniczna fazy 2 TREM2-agonisty AL002 wykazała utrzymane zaangażowanie celu i odpowiedź farmakodynamiczną w PMR, ale nie osiągnęła pierwotnego punktu końcowego klinicznego (zmiana CDR-SB), a częstym działaniem niepożądanym były zmiany MRI przypominające ARIA. Oznacza to, że biomarkerowa „aktywacja mikrogleju” nie gwarantuje skuteczności klinicznej, a ryzyko działań niepożądanych może być związane z immunologiczną komponentą terapii (Mummery i in., 2026).
Komentarz poświęcony „porażce INVOKE-2” podkreśla, że TREM2 pozostaje biologicznie istotne, ale prawdopodobnie wymaga lepszego zrozumienia: kiedy wzmacniać mikroglej (fazy wczesne?), a kiedy hamować szkodliwe osie (np. dopełniacz), jak dobierać pacjentów (fenotyp zapalny/BBB), i jakie punkty końcowe uznawać za adekwatne (Colonna i Holtzman, 2025).
Interwencje ukierunkowane na dopełniacz (np. C5aR1) są na razie lepiej udokumentowane przedklinicznie niż klinicznie. Dane z modeli mysich sugerują, że hamowanie osi C5aR1 może ograniczać szkodliwe odpowiedzi glialne i poprawiać funkcje poznawcze, ale literatura podkreśla potrzebę precyzyjnego „celowania” (który komponent dopełniacza, w jakim etapie choroby) (Schartz i in., 2024; Zelek i in., 2025).
Poziom dowodów: wysoki (RCT) dla braku skuteczności klinicznej TREM2-agonisty AL002 przy potwierdzonych efektach farmakodynamicznych; umiarkowany dla koncepcji immunomodulacji dopełniacza (silne dane przedkliniczne, ograniczone kliniczne).
Interwencje stylu życia i „osie obwodowe” neurozapalania
W obszarze prewencji i spowalniania spadku funkcji poznawczych rośnie znaczenie interwencji wielodomenowych. Badanie FINGER wykazało, że 2-letnia interwencja obejmująca m.in. dietę, aktywność fizyczną, trening poznawczy i kontrolę czynników naczyniowych może poprawiać lub utrzymywać funkcjonowanie poznawcze u osób starszych z podwyższonym ryzykiem (Ngandu i in., 2015). Choć FINGER nie jest „badaniem neurozapalania” sensu stricto, jest mocnym argumentem, że czynniki modyfikowalne (często powiązane ze stanem zapalnym i naczyniowym) przekładają się na twarde wyniki poznawcze (Ngandu i in., 2015).
W obszarze diety, randomizowane badania osadzone w programie PREDIMED wskazywały na korzystne efekty diety śródziemnomorskiej wzbogaconej oliwą z oliwek lub orzechami na funkcje poznawcze, co jest spójne z hipotezą o roli komponentów prozdrowotnych o działaniu m.in. przeciwzapalnym i naczynioprotekcyjnym (Valls-Pedret i in., 2015). Metaanalizy obserwacyjne potwierdzają związek wysokiej adherencji do diety śródziemnomorskiej z niższym ryzykiem zaburzeń poznawczych i otępienia, choć nie rozstrzygają mechanizmu (Fekete i in., 2025).
Aktywność fizyczna redukuje systemowe markery zapalne u osób starszych w metaanalizach badań interwencyjnych (m.in. spadki CRP i TNF-α, słabsze i bardziej zależne od kontekstu efekty dla IL-6). To jest istotne, bo systemowa „niska zapalność” jest rozważana jako modulator BBB i odpowiedzi mikrogleju, choć przełożenie na neurozapalanie w mózgu wymaga ostrożności interpretacyjnej (Khalafi i in., 2023).
W zakresie snu dane kohortowe i metaanalizy wskazują, że zaburzenia snu są związane ze zwiększonym ryzykiem chorób neurodegeneracyjnych, a ryzyko może być widoczne wiele lat przed rozpoznaniem klinicznym. Mechanistycznie rozważa się m.in. osłabienie procesów „oczyszczania” i modulację osi zapalnych, ale nie jest to jednoznacznie rozstrzygnięte (Simmonds i in., 2025; Zhang i in., 2025).
Poziom dowodów: wysoki (RCT) dla wielodomenowych interwencji poprawiających/utrzymujących funkcje poznawcze w grupach ryzyka (FINGER); umiarkowany dla bezpośredniego „wyciszenia neurozapalania w mózgu” jako mechanizmu; umiarkowany–wysoki dla redukcji systemowych markerów zapalnych przez ćwiczenia (metaanalizy RCT); umiarkowany dla relacji sen–neurodegeneracja (metaanalizy i dane biobankowe, ale mechanizm przyczynowy wieloczynnikowy).
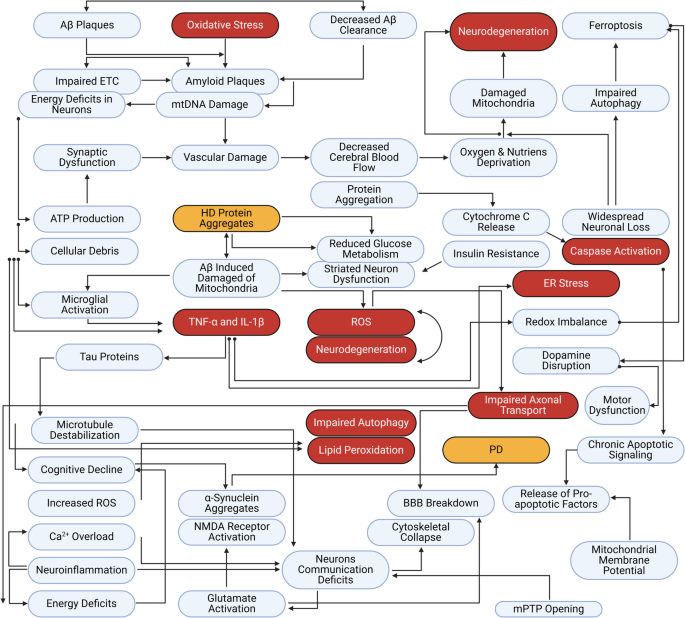
Wykres relacji między neurozapalaniem a mechanizmami neurodegeneracji
mermaidKopiujflowchart TD
A[Wyzwalacze: agregaty bialek (Abeta, tau, alfa-syn), uraz, infekcja, starzenie] --> B[PRR: TLR i inne receptory rozpoznania zagrozenia]
B --> C[NF-kB: ekspresja genow prozapalnych]
C --> D[Wydzielanie cytokin/chemokin: IL-1b, IL-6, TNF, MCP-1]
C --> E[Priming NLRP3]
E --> F[NLRP3: kaspaza-1 -> IL-1b/IL-18, pyroptoza]
D --> G[Aktywacja mikrogleju i astrocytow]
G --> H[Dopełniacz (C1q/C3/C5a): tagowanie synaps]
H --> I[Pruning synaps przez mikroglej]
G --> J[Stres oksydacyjny i dysfunkcja mitochondrialna]
D --> K[Dysfunkcja BBB]
K --> L[Wnikanie mediatorow i komorek odpornosci z obwodu]
L --> D
I --> M[Dysfunkcja sieci neuronalnych i objawy]
J --> N[Uszkodzenie neuronow i progresja neurodegeneracji]
N --> A
Model ten pokazuje typowy układ sprzężeń zwrotnych: uszkodzenie i agregaty białkowe nasilają odpowiedź wrodzoną (TLR/NF-κB/NLRP3), która poprzez cytokiny, dopełniacz i dysfunkcję BBB może dalej przyspieszać utratę synaps i neuronów (Heneka i in., 2015; Hong i in., 2016; Shin i in., 2026).
Luki w wiedzy i kierunki badań
Największą luką jest niedostateczne rozdzielenie fenotypów ochronnych i szkodliwych oraz niedostateczna wiedza „kiedy” interweniować. Zarówno mikroglej, jak i astrocyty wykazują dynamiczne przeprogramowanie w czasie choroby, a pojedyncza strategia (np. globalne pobudzenie mikrogleju lub globalne hamowanie zapalenia) może być biologicznie nieadekwatna (Gao i in., 2023; Mummery i in., 2026).
Drugą luką jest stratyfikacja pacjentów: neurodegeneracja to zespół procesów, a nie jedna choroba na poziomie biologii. Ważne pytanie brzmi, czy istnieją podtypy (np. „immuno-dominujące”, „naczyniowe”, „metaboliczne”), które w większym stopniu skorzystają na terapii immunomodulacyjnej. Wymaga to paneli biomarkerów (glialnych, BBB, proteomicznych) i projektów badań klinicznych opartych o biologiczne kryteria włączenia (Heneka i in., 2025; Brosseron i in., 2018).
Trzecim kierunkiem jest integracja danych single-cell i multi-omics w neurozapalaniu: techniki te pozwalają mapować odpowiedzi komórkowe w skali pojedynczej komórki i lepiej identyfikować cele „na etapie” (np. szlaki w mikrogleju specyficzne dla fazy prodromalnej vs fazy otępiennej). To może przełożyć się na precyzyjniejsze leki oraz lepsze wskaźniki odpowiedzi (Ingelfinger i in., 2022; Lassmann, 2022).
Czwartą luką jest przełożenie skuteczności farmakodynamicznej na kliniczną. Próba AL002 szczególnie wyraźnie pokazuje, że nawet jeśli biomarkery potwierdzają „trafienie” w cel i zmianę sygnalizacji, nie musi to skutkować poprawą kliniczną – co sugeruje, że cel był nieadekwatny, etap choroby zbyt późny, punkt końcowy zbyt mało czuły lub że istnieją kompensacje biologiczne (Mummery i in., 2026; Colonna i Holtzman, 2025).
Poziom dowodów: wysoki dla istnienia heterogenności biologicznej (single-cell i przeglądy), umiarkowany dla konkretnych strategii jej wykorzystania klinicznie (w trakcie rozwoju).
Kluczowe artykuły i ich znaczenie
- Ransohoff (2016) – syntetyczna definicja neurozapalania jako procesu kształtującego środowisko neuronu; rama pojęciowa dla myślenia o „glio-naczyniowym” wkładzie w neurodegenerację. (Poziom: przegląd – integracja kliniczno-mechanistyczna).
- Heneka i in. (2015) – klasyczny przegląd neurozapalania w AD łączący agregaty białkowe, PRR, mikroglej/astroglej i ryzyko genetyczne. (Poziom: przegląd eksperymentalno-kliniczny).
- Bellenguez i in. (2022) – duże GWAS z podkreśleniem roli mikrogleju/odporności w ryzyku AD. (Poziom: genetyka populacyjna).
- Kunkle i in. (2019) – metaanaliza GWAS AD wskazująca na odporność jako jeden z kluczowych obszarów ryzyka biologicznego. (Poziom: genetyka populacyjna).
- Heneka i in. (2013) – dowód przyczynowy w modelu APP/PS1: NLRP3/kaspaza-1 wpływają na patologię i funkcje poznawcze. (Poziom: eksperymentalny, mocny).
- Hong i in. (2016) – mechanizm dopełniaczowego tagowania i eliminacji synaps przez mikroglej jako ścieżka utraty synaps w neurodegeneracji. (Poziom: eksperymentalny, przełomowy).
- Liddelow i in. (2017) – identyfikacja sygnałów mikroglejowych indukujących neurotoksyczne astrocyty; most między cytokinami i dopełniaczem. (Poziom: eksperymentalny).
- Swardfager i in. (2010) – metaanaliza cytokin w AD; pokazuje globalny sygnał prozapalny, ale też heterogeniczność danych. (Poziom: metaanaliza kliniczna).
- Qin i in. (2016) – metaanaliza markerów zapalnych w PD, podstawa do krytycznej oceny biomarkerów cytokinowych. (Poziom: metaanaliza kliniczna).
- Hu i in. (2017) – metaanaliza cytokin we krwi w ALS; sygnał zapalny obecny, ale zmienny. (Poziom: metaanaliza kliniczna).
- Kim i in. (2023) – metaanaliza GFAP jako biomarkera krwi w AD; ważny krok w kierunku testów mniej inwazyjnych. (Poziom: przegląd systematyczny/metaanaliza).
- Mummery i in. (2026) – faza 2 AL002: modelowy przykład rozjazdu między farmakodynamiką (cel) a skutecznością kliniczną; istotne dane o ARIA. (Poziom: RCT, wysoki).
- Ngandu i in. (2015) – FINGER: dowód, że wielodomenowe modyfikacje stylu życia wpływają na funkcje poznawcze u osób zagrożonych; ważny filar prewencji. (Poziom: RCT, wysoki).
- De Picker i in. (2023) – metaanaliza TSPO-PET: ocena użyteczności obrazowania neurozapalania w różnych chorobach i kluczowych ograniczeń metody. (Poziom: przegląd systematyczny/metaanaliza).
Wnioski i implikacje kliniczne
Neurozapalanie jest obecnie najlepiej rozumiane jako dynamiczny, wielokomórkowy i wieloszlakowy proces regulujący środowisko neuronu. W AD dowody są najsilniejsze dzięki zbieżności genetyki populacyjnej, mechanizmów eksperymentalnych (NLRP3, dopełniacz) i biomarkerów glialnych. W PD i ALS obraz jest spójny co do obecności komponenty zapalnej, ale mniej rozstrzygający co do kierunku przyczynowości i najlepszego celu terapeutycznego (Heneka i in., 2015; Bellenguez i in., 2022; Qin i in., 2016; Hu i in., 2017).
Praktycznie klinika stoi dziś w punkcie, w którym: (1) biomarkery glialne (GFAP, sTREM2, YKL-40) i TSPO-PET coraz częściej wspierają badania i stratyfikację, ale (2) większość szerokich terapii przeciwzapalnych w chorobie jawnej nie działa, a nawet nowoczesne immunomodulatory (np. TREM2-agonista) mogą nie poprawiać klinicznie mimo zmian biomarkerów. Implikuje to, że skuteczne leczenie będzie wymagało lepszego dopasowania mechanizmu do etapu choroby i fenotypu biologicznego pacjenta (Brosseron i in., 2018; Mummery i in., 2026; Heneka i in., 2025).
W perspektywie praktyki klinicznej najbardziej obiecującym kierunkiem jest „medycyna warstwowa”: łączenie oceny klasycznych markerów neurodegeneracji (Aβ/tau/NfL), markerów glialnych i naczyniowych (GFAP, sTREM2, sPDGFRβ) oraz danych klinicznych o obwodowym stanie zapalnym (choroby autoimmunologiczne, czynniki naczyniowe, sen, aktywność fizyczna). Taka integracja ma szansę wskazać pacjentów, u których immunomodulacja ma największe prawdopodobieństwo sensu biologicznego – oraz pozwolić monitorować odpowiedź w sposób bardziej bezpośredni niż sama skala kliniczna (Heneka i in., 2025; Miners i in., 2019; Kim i in., 2023).
Bibliografia
Badawoud, A. M., et al. (2024). The relation between Parkinson’s disease and non-steroidal anti-inflammatories: A systematic review and meta-analysis. Frontiers in Pharmacology.
Batista, A. F., et al. (2024). The importance of complement-mediated immune mechanisms in Alzheimer’s disease. International Journal of Molecular Sciences.
Bellenguez, C., et al. (2019). Genetic meta-analysis of diagnosed Alzheimer’s disease identifies new risk loci and implicates Aβ, tau, immunity and lipid processing. Nature Genetics, 51, 414–430.
Bellenguez, C., et al. (2022). New insights into the genetic etiology of Alzheimer’s disease and related dementias. Nature Genetics.
Biswas, K., et al. (2023). A review on the cell signaling pathways involved in microglial activation. (PubMed-indexed review).
Brosseron, F., Traschütz, A., Widmann, C. N., et al. (2018). Characterization and clinical use of inflammatory cerebrospinal fluid protein markers in Alzheimer’s disease. Alzheimer’s Research & Therapy, 10, 25.
Blevins, H. M., et al. (2022). The NLRP3 inflammasome pathway: A review of mechanisms and therapeutics. Frontiers in Immunology / PMC.
Colonna, M., & Holtzman, D. M. (2025). Rethinking TREM2 as a target for Alzheimer’s disease after the INVOKE-2 trial failure. Nature Medicine, 31(10), 3217–3218.
Craig-Schapiro, R., Perrin, R. J., Roe, C. M., et al. (2010). YKL-40: A novel prognostic fluid biomarker for preclinical Alzheimer’s disease. Biological Psychiatry.
Dabi, Y. T., et al. (2023). Toll-like receptors in pathogenesis of neurodegenerative diseases. Immunity, Inflammation and Disease.
De Picker, L. J., et al. (2023). TSPO PET brain inflammation imaging: A transdiagnostic systematic review and meta-analysis. NeuroImage / PubMed.
Deczkowska, A., et al. (2018). Disease-associated microglia: A universal immune sensor of neurodegeneration. Cell.
Fekete, M., et al. (2025). The role of the Mediterranean diet in reducing the risk of age-related cognitive disorders: A meta-analysis. GeroScience.
Galea, E., et al. (2023). Neuroinflammation: The abused concept. Cellular Neuroscience / PubMed-indexed article.
Gao, C., et al. (2023). Microglia in neurodegenerative diseases: Mechanism and therapy. Signal Transduction and Targeted Therapy.
Gao, X., et al. (2011). Use of ibuprofen and risk of Parkinson disease. (PubMed-indexed cohort study).
Gordon, P. H., et al. (2007). Efficacy of minocycline in patients with amyotrophic lateral sclerosis: A phase III randomised trial. The Lancet Neurology, 6(12), 1045–1053.
Han, Q. Q., et al. (2023). NLRP3 inflammasome-mediated neuroinflammation and mitochondrial impairment during Parkinson’s disease progression. (PMC review).
Heneka, M. T., et al. (2013). NLRP3 is activated in Alzheimer’s disease and contributes to pathology in APP/PS1 mice. Nature.
Heneka, M. T., et al. (2015). Neuroinflammation in Alzheimer’s disease. The Lancet Neurology.
Heneka, M. T., et al. (2025). Neuroinflammatory fluid biomarkers in patients with Alzheimer’s disease: systematic literature review. (Peer-reviewed SLR).
Holbrook, J. A., et al. (2021). Neurodegenerative disease and the NLRP3 inflammasome. Frontiers in Pharmacology.
Howard, R., et al. (2019/2020). Minocycline at 2 different dosages vs placebo for patients with mild Alzheimer disease: A randomized clinical trial. (Randomized clinical trial).
Hu, Y., et al. (2017). Increased peripheral blood inflammatory cytokine levels in amyotrophic lateral sclerosis: A meta-analysis study. Scientific Reports.
Ingelfinger, F., et al. (2022). Single-cell multiomics in neuroinflammation. Trends in Immunology.
Keren-Shaul, H., et al. (2017). A unique microglia type associated with restricting development of Alzheimer’s disease. Cell.
Khalafi, M., et al. (2023). Exercise training and inflammatory biomarkers in older adults: Systematic review and meta-analysis. (Peer-reviewed SR/MA).
Kim, K. Y., et al. (2023). GFAP as a potential biomarker for Alzheimer’s disease: Systematic review and meta-analysis. Cells.
Krasemann, S., et al. (2017). The TREM2-APOE pathway drives the transcriptional phenotype of dysfunctional microglia in neurodegenerative diseases. Immunity.
Lai, K. S. P., et al. (2017). Peripheral inflammatory markers in Alzheimer’s disease: A systematic review and meta-analysis of 175 studies. Journal of Neurology, Neurosurgery & Psychiatry, 88, 876–882.
Lassmann, H. (2022). Neuroinflammation: 2022 update. Free Neuropathology.
Liddelow, S. A., et al. (2017). Neurotoxic reactive astrocytes are induced by activated microglia. Nature.
Lyketsos, C. G., et al. (2007). Naproxen and celecoxib do not prevent Alzheimer dementia in early results from a randomized controlled trial. Neurology.
Martin, B. K., et al. (2008). Cognitive function over time in the Alzheimer’s Disease Anti-inflammatory Prevention Trial (ADAPT). Archives of Neurology.
Miners, J. S., Kehoe, P. G., Love, S., Zetterberg, H., & Blennow, K. (2019). CSF evidence of pericyte damage in Alzheimer’s disease is associated with markers of blood–brain barrier dysfunction and disease pathology. Alzheimer’s Research & Therapy, 11, 81.
Mummery, C. J., Mayorga, A. J., Simmons, A., et al. (2026). The TREM2 agonistic antibody AL002 in early Alzheimer’s disease: a phase 2 randomized trial. Nature Medicine.
Ngandu, T., et al. (2015). A 2 year multidomain intervention of diet, exercise, cognitive training, and vascular risk monitoring versus control to prevent cognitive decline in at-risk elderly people (FINGER): a randomised controlled trial. The Lancet, 385, 2255–2263.
Papavergi, M. T., et al. (2025). The complement cascade in Alzheimer’s disease: modern mechanisms and therapeutic opportunities. Molecular Neurodegeneration / Springer.
Peter, I., et al. (2018). Anti–tumor necrosis factor therapy and incidence of Parkinson disease among patients with inflammatory bowel disease. JAMA Neurology.
Potashman, M., et al. (2025). The impact of anti-inflammatory therapy on Parkinson’s disease risk: effects of anti-TNF and anti-IL-17. (Peer-reviewed cohort analysis).
Qin, X.-Y., et al. (2016). Inflammatory biomarkers in Parkinson’s disease: A systematic review and meta-analysis. (PubMed-indexed SR/MA).
Ransohoff, R. M. (2016). How neuroinflammation contributes to neurodegeneration. Science, 353(6301), 777–783.
Roveta, F., et al. (2024). Neuroinflammatory biomarkers in Alzheimer’s disease. International Journal of Molecular Sciences.
Schartz, N. D., et al. (2024). C5aR1 antagonism suppresses inflammatory glial responses and alters cellular signaling in an Alzheimer’s disease mouse model. (PMC preclinical study).
Shi, F. D., et al. (2025). Neuroinflammation across neurological diseases. Science.
Shin, H. J., et al. (2026). Molecular mechanisms of NLRP3 inflammasome activation. Experimental & Molecular Medicine / Nature.
Squillace, S., et al. (2022). Toll-like receptor-mediated neuroinflammation. (PMC review).
Swardfager, W., et al. (2010). A meta-analysis of cytokines in Alzheimer’s disease. Biological Psychiatry.
Sweeney, M. D., et al. (2020). A novel sensitive assay for detection of a biomarker of blood–brain barrier dysfunction (PDGFRβ/sPDGFRβ). (PubMed-indexed biomarker study).
Valls-Pedret, C., et al. (2015). Mediterranean diet and age-related cognitive decline: A randomized clinical trial (PREDIMED). JAMA Internal Medicine.
Wang, R., et al. (2024). Association of soluble TREM2 with Alzheimer’s disease and mild cognitive impairment: A systematic review and meta-analysis. Frontiers in Aging Neuroscience.
Zelek, W. M., et al. (2025). Complement therapeutics in neurodegenerative diseases. (Peer-reviewed review).
Zhang, J., et al. (2025). Sleep disorders and the risk of cognitive decline or dementia: Updated systematic review and meta-analysis. Journal of Neurology.
Zhang, W., et al. (2023). Role of neuroinflammation in neurodegeneration. Signal Transduction and Targeted Therapy.
Opracowanie: Rafał Klasiński / Independent Institute of Chemical Processes